Кетонові тіла виробляються печінкою і використовуються як джерело енергії, коли глюкоза недоступна в організмі людини. Двома основними кетоновими тілами є ацетоацетат (AcAc) і 3-бета-гідроксибутират (3HB), тоді як ацетон є третім і найменш поширеним кетоновим тілом. Кетони завжди присутні в крові, і їх рівень підвищується під час голодування і тривалих фізичних навантажень.�Кетогенез це біохімічний процес, за допомогою якого організми виробляють кетонові тіла шляхом розщеплення жирних кислот і кетогенних амінокислот.
Кетонові тіла в основному утворюються в мітохондрії клітин печінки. Кетогенез відбувається, коли в крові низький рівень глюкози, особливо після того, як інші клітинні запаси вуглеводів, наприклад глікоген, були вичерпані. Цей механізм також може виникнути при недостатній кількості інсуліну. Виробництво кетонових тіл в кінцевому підсумку ініціюється, щоб зробити доступною енергію, яка зберігається в організмі людини у вигляді жирних кислот. Кетогенез відбувається в мітохондріях, де він регулюється незалежно.
зміст
абстрактний
Метаболізм кетонових тіл є центральним вузлом фізіологічного гомеостазу. У цьому огляді ми обговорюємо, як кетони виконують дискретні метаболічні функції, які оптимізують роботу органів і організмів у різних залишках поживних речовин і захищають від запалення та травм у багатьох системах органів. Традиційно розглядаються як метаболічні субстрати, які беруть участь лише при обмеженні вуглеводів, нещодавні спостереження підкреслюють важливість кетонових тіл як життєво важливих метаболічних і сигнальних медіаторів, коли вуглеводи є у великій кількості. Доповнюючи репертуар відомих терапевтичних можливостей для захворювань нервової системи, виникла перспективна роль кетонових тіл при раку, а також інтригуючі захисні ролі в серці та печінці, відкриваючи терапевтичні можливості при ожирінні та серцево-судинних захворюваннях. Для узгодження класичної догми з сучасними спостереженнями обговорюються суперечності в метаболізмі кетонів і передачі сигналів.
Вступ
Кетонові тіла є життєво важливим альтернативним джерелом метаболічного палива для всіх сфер життя, еукарії, бактерій та архей (Aneja et al., 2002; Cahill GF Jr, 2006; Krishnakumar et al., 2008). Метаболізм кетонових тіл у людей був використаний для підживлення мозку під час епізодичних періодів нестачі поживних речовин. Кетонові тіла переплетені з ключовими метаболічними шляхами ссавців, такими як ?-окислення (FAO), цикл трикарбонових кислот (TCA), глюконеогенез, de novo ліпогенез (DNL) і біосинтез стеролів. У ссавців кетонові тіла виробляються переважно в печінці з ацетил-КоА, що походить від ФАО, і вони транспортуються до позапечінкових тканин для кінцевого окислення. Ця фізіологія забезпечує альтернативне паливо, яке доповнюється відносно короткими періодами голодування, що збільшує доступність жирних кислот і зменшує доступність вуглеводів (Cahill GF Jr, 2006; McGarry and Foster, 1980; Robinson and Williamson, 1980). Окислення кетонових тіл стає важливим фактором загального енергетичного метаболізму ссавців у позапечінкових тканинах у безлічі фізіологічних станів, включаючи голодування, голодування, період новонародженості, після тренування, вагітність та дотримання дієти з низьким вмістом вуглеводів. У здорових дорослих людей загальні концентрації кетонових тіл у циркуляції зазвичай мають циркадні коливання між приблизно 100-250 мМ, підвищуються до ~1 мМ після тривалих фізичних навантажень або 24-годинного голодування і можуть накопичуватися до 20 мМ при таких патологічних станах, як діабетичний кетоацидоз ( Cahill GF Jr, 2006; Johnson et al., 1969b; Koeslag та ін., 1980; Robinson and Williamson, 1980; Wildenhoff та ін., 1974). Печінка людини виробляє до 300 г кетонових тіл на добу (Balasse and Fery, 1989), які вносять від 5 до 20% загальних витрат енергії при нагодуванні, голодуванні та голодуванні (Balasse et al., 1978; Cox et al. ін., 2016).
Недавні дослідження висвітлюють важливу роль кетонових тіл у метаболізмі клітин ссавців, гомеостазі та передачі сигналів у широкому діапазоні фізіологічних та патологічних станів. Окрім того, що вони служать енергетичним паливом для позапечінкових тканин, таких як мозок, серце або скелетні м’язи, кетонові тіла відіграють ключову роль як сигнальні медіатори, рушії посттрансляційної модифікації білка (PTM) і модулятори запалення та окислювального стресу. У цьому огляді ми надаємо як класичні, так і сучасні погляди на плейотропну роль кетонових тіл та їх метаболізм.
Огляд метаболізму кетонового тіла
Швидкість кетогенезу печінки регулюється організованою серією фізіологічних і біохімічних перетворень жиру. Основні регулятори включають ліполіз жирних кислот з триацилгліцеринів, транспортування до плазматичної мембрани гепатоцитів і через неї, транспортування в мітохондрії за допомогою карнітинпальмітоілтрансферази 1 (CPT1), спіраль β-окислення, активність циклу TCA та проміжні концентрації, потенціал окисно-відновного регулювання та гормональний регуляторний потенціал. з цих процесів, переважно глюкагон та інсулін [огляд в (Arias et al., 1995; Ayte et al., 1993; Ehara et al., 2015; Ferre et al., 1983; Kahn et al., 2005; McGarry and Foster , 1980; Williamson et al., 1969)]. Класично кетогенез розглядають як шлях поширення, при якому ацетил-КоА, отриманий від α-окислення, перевищує активність цитратсинтази та/або доступність оксалоацетату для конденсації з утворенням цитрату. Тривуглецеві проміжні продукти виявляють антикетогенну активність, імовірно, через їхню здатність розширювати пул оксалоацетату для споживання ацетил-КоА, але сама концентрація ацетил-КоА в печінці не визначає швидкість кетогенезу (Foster, 1967; Rawat and Menahan, 1975; Williamson та ін., 1969). Регулювання кетогенезу гормональними, транскрипційними та посттрансляційними подіями разом підтверджує думку про те, що молекулярні механізми, які точно регулюють швидкість кетогенезу, залишаються неповністю зрозумілими (див. Регулювання HMGCS2 і SCOT/OXCT1).
Кетогенез відбувається переважно в мітохондріальному матриксі печінки зі швидкістю, пропорційною до загального окислення жиру. Після транспортування ацильних ланцюгів через мітохондріальні мембрани та ?-окислення мітохондріальна ізоформа 3-гідроксиметилглутарил-КоА-синтази (HMGCS2) каталізує долю, в результаті чого відбувається конденсація ацетоацетил-КоА (AcAc-CoA) і утворення HMG-Ac-CoA. (рис. 1А). HMG-CoA ліаза (HMGCL) розщеплює HMG-CoA з вивільненням ацетил-КоА та ацетоацетату (AcAc), а останній відновлюється до d-?-гідроксибутирату (d-?OHB) за допомогою фосфатидилхолін-залежної мітохондріальної d-?OHB дегідрогенази. BDH1) у близькорівноважній реакції, пов’язаної з NAD+/NADH (Bock and Fleischer, 1975; LEHNINGER et al., 1960). Константа рівноваги BDH1 сприяє виробленню d-?OHB, але співвідношення кетонових тіл AcAc/d-?OHB прямо пропорційне відношенню мітохондріальних NAD+/NADH, і, таким чином, активність оксидоредуктази BDH1 модулює окислювально-відновний потенціал мітохондрій (Krebs et al., 1969; Вільямсон та ін., 1967). AcAc також може спонтанно декарбоксилюватися до ацетону (Pedersen, 1929), джерела солодкого запаху у людей, які страждають на кетоацидоз (тобто загальна кількість кетонових тіл сироватки > ~7 мМ; AcAc pKa 3.6, ?OHB pKa 4.7). Механізми, за допомогою яких кетонові тіла транспортуються через внутрішню мембрану мітохондрій, невідомі, але AcAc/d-?OHB вивільняються з клітин за допомогою монокарбоксилатних транспортерів (у ссавців MCT 1 і 2, також відомі як переносники розчиненої речовини 16A, члени сімейства 1 і 7) і транспортується в кровообігу до позапечінкових тканин для термінального окислення (Cotter et al., 2011; Halestrap and Wilson, 2012; Halestrap, 2012; Hugo et al., 2012). Концентрації циркулюючих кетонових тіл вищі, ніж у позапечінкових тканинах (Harrison and Long, 1940), що вказує на те, що кетонові тіла транспортуються вниз за градієнтом концентрації. Мутації втрати функції в MCT1 пов’язані зі спонтанними нападами кетоацидозу, що свідчить про вирішальну роль в імпорті кетонових тіл.
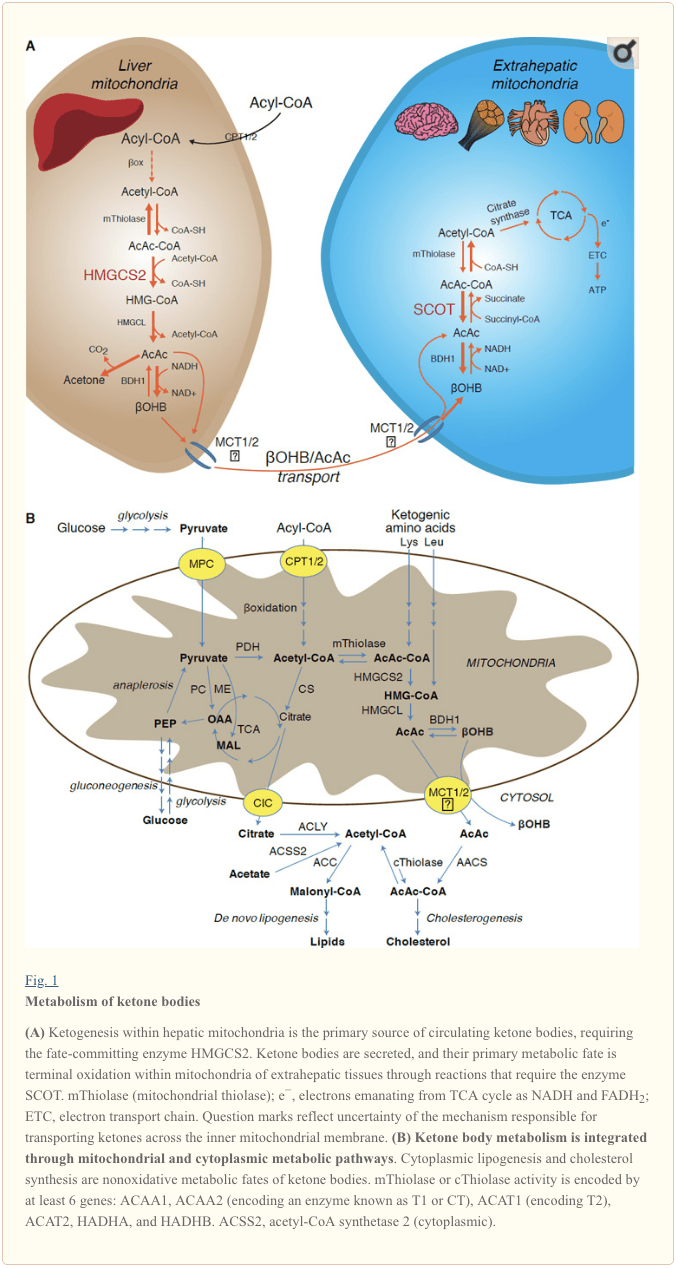
� За винятком можливого переведення кетонових тіл у неокислювальні долі (див. Неокислювальні метаболічні долі кетонових тіл), гепатоцити не мають здатності метаболізувати кетонові тіла, які вони виробляють. Кетонові тіла, синтезовані печінкою de novo, (i) катаболізуються в мітохондріях позапечінкових тканин до ацетил-КоА, який доступний для циклу TCA для кінцевого окислення (рис. 1A), (ii) направляється на шляхи ліпогенезу або синтезу стеролів ( Рис. 1B), або (iii) виводиться із сечею. Як альтернативне енергетичне паливо, кетонові тіла жадібно окислюються в серці, скелетних м’язах і мозку (Balasse and Fery, 1989; Bentourkia et al., 2009; Owen et al., 1967; Reichard et al., 1974; Sultan, 1988 ). Позапечінковий мітохондріальний BDH1 каталізує першу реакцію окислення ?OHB, перетворюючи його в зворотний AcAc (LEHNINGER et al., 1960; Sandermann et al., 1986). Цитоплазматична d-?OHB-дегідрогеназа (BDH2) з ідентичністю послідовності лише на 20% з BDH1 має високу Km для кетонових тіл, а також відіграє роль у гомеостазі заліза (Davuluri et al., 2016; Guo et al., 2006) . У позапечінковому мітохондріальному матриксі AcAc активується до AcAc-CoA шляхом обміну CoA-частиною з сукциніл-CoA в реакції, що каталізується унікальною CoA трансферазою ссавців, сукциніл-CoA:3-oxoacid-CoA трансферазою (SCOT, CoA transferase; кодується OXCT1) через реакцію, близьку до рівноваги. Вільна енергія, що виділяється при гідролізі AcAc-CoA, більша, ніж сукциніл-CoA, що сприяє утворенню AcAc. Таким чином, окислювальний потік кетонових тіл відбувається внаслідок дії маси: рясний запас AcAc і швидке споживання ацетил-КоА через цитратсинтазу сприяє утворенню AcAc-CoA (+ сукцинат) SCOT. Примітно, що на відміну від глюкози (гексокінази) і жирних кислот (ацил-КоА-синтетаз), активація кетонових тіл (СКОТ) у форму, що окислюється, не вимагає вкладення АТФ. Зворотна реакція тіолази AcAc-CoA [що каталізується будь-якою з чотирьох мітохондріальних тіолаз, що кодуються ACAA2 (кодує фермент, відомий як T1 або CT), ACAT1 (кодує T2), HADHA або HADHB], дає дві молекули ацетил-CoA які входять у цикл TCA (Hersh і Jencks, 1967; Stern et al., 1956; Williamson et al., 1971). Під час кетотичних станів (тобто загальні кетони сироватки > 500 мкМ) кетонові тіла стають значним внеском у витрати енергії і швидко використовуються в тканинах, поки не відбувається поглинання або насичення окислення (Balasse et al., 1978; Balasse and Fery, 1989 Едмонд та ін., 1987). Дуже невелику частку кетонових тіл, отриманих з печінки, можна легко виміряти в сечі, а швидкість утилізації та реабсорбції нирками пропорційна концентрації в крові (Goldstein, 1987; Robinson and Williamson, 1980). Під час високо кетотичних станів (> 1 мМ у плазмі) кетонурія служить напівкількісним звітом про кетоз, хоча більшість клінічних аналізів кетонових тіл у сечі виявляє AcAc, але не ?OHB (Klocker et al., 2013).
Кетогенні субстрати та їх вплив на метаболізм гепатоцитів
Кетогенні субстрати включають жирні кислоти та амінокислоти (рис. 1В). Катаболізм амінокислот, особливо лейцину, утворює близько 4% кетонових тіл у стані після абсорбції (Thomas et al., 1982). Таким чином, пул субстратів ацетил-КоА для утворення кетонових тіл в основному походить з жирних кислот, оскільки під час станів зниженого постачання вуглеводів піруват потрапляє в печінковий цикл TCA переважно через анаплероз, тобто АТФ-залежне карбоксилування до оксалоацетату (OAA) або до малату. (MAL), а не окисне декарбоксилювання до ацетил-КоА (Jeoung et al., 2012; Magnusson et al., 1991; Merritt et al., 2011). У печінці глюкоза та піруват мізерно сприяють кетогенезу, навіть коли декарбоксилювання пірувату до ацетил-КоА є максимальним (Jeoung et al., 2012).
Ацетил-КоА відіграє кілька ролей, невід'ємних від проміжного метаболізму в печінці, крім генерації АТФ через кінцеве окислення (також див. Інтеграція метаболізму кетонових тіл, посттрансляційної модифікації та фізіології клітин). Ацетил-КоА алостерично активує (i) піруваткарбоксилазу (PC), тим самим активуючи механізм метаболічного контролю, який посилює анаплеротичний надходження метаболітів у цикл TCA (Owen et al., 2002; Scrutton and Utter, 1967) і (ii) дегідрогеназу. кіназа, яка фосфорилює та інгібує піруватдегідрогеназу (PDH) (Cooper et al., 1975), тим самим ще більше посилюючи потік пірувату в цикл TCA через анаплероз. Крім того, цитоплазматичний ацетил-КоА, пул якого збільшується механізмами, які перетворюють мітохондріальний ацетил-КоА в транспортні метаболіти, інгібує окислення жирних кислот: ацетил-КоА-карбоксилаза (ACC) каталізує перетворення ацетил-КоА в малоніл-КоА, ліпогенний субстрат. та алостеричний інгібітор мітохондріального CPT1 [огляд у (Kahn et al., 2005; McGarry and Foster, 1980)]. Таким чином, мітохондріальний пул ацетил-КоА як регулює, так і регулюється переливним шляхом кетогенезу, який керує ключовими аспектами печінкового проміжного метаболізму.
Неокислювальні метаболічні долі кетонових тіл
Переважна доля кетонів, отриманих з печінки, - це SCOT-залежне позапечінкове окислення. Однак AcAc може експортуватися з мітохондрій і використовуватися в анаболічних шляхах шляхом перетворення в AcAc-CoA за допомогою АТФ-залежної реакції, що каталізується цитоплазматичною ацетоацетил-КоА-синтетазою (AACS, рис. 1B). Цей шлях активний під час розвитку мозку та в молочних залозах лактації (Morris, 2005; Robinson and Williamson, 1978; Ohgami et al., 2003). AACS також високо експресується в жировій тканині та активованих остеокластах (Aguilo et al., 2010; Yamasaki et al., 2016). Цитоплазматичний AcAc-CoA може бути або спрямований цитозольним HMGCS1 на біосинтез стеролів, або розщепленим будь-якою з двох цитоплазматичних тіолаз до ацетил-КоА (ACAA1 і ACAT2), карбоксилювати до малоніл-КоА і сприяти синтезу жирних кислот та ін. ін., 1984; Едмонд, 1974; Ендеманн та ін., 1982; Джілен та ін., 1983; Веббер і Едмонд, 1977).
Хоча фізіологічне значення ще не встановлено, кетони можуть служити анаболічним субстратом навіть у печінці. У штучних експериментальних контекстах AcAc може вносити до половини новосинтезованих ліпідів і до 75% нового синтезованого холестерину (Endemann et al., 1982; Geelen et al., 1983; Freed et al., 1988). Оскільки AcAc походить від неповного окислення жирів у печінці, здатність AcAc сприяти ліпогенезу in vivo означатиме безперспективний цикл у печінці, коли кетони, отримані з жиру, можуть бути використані для виробництва ліпідів, поняття, фізіологічне значення якого вимагає експериментального підтвердження, але може служити адаптивні або дезадаптивні ролі (Solinas et al., 2015). AcAc активно забезпечує холестерогенез з низьким вмістом AACS Km-AcAc (~50 мкМ), що сприяє активації AcAc навіть у стані нагодування (Bergstrom et al., 1984). Динамічну роль цитоплазматичного метаболізму кетонів припускають у первинних ембріональних нейронах миші та в адипоцитах, отриманих від 3T3-L1, оскільки нокдаун AACS порушує диференціацію кожного типу клітин (Hasegawa et al., 2012a; Hasegawa et al., ). Нокдаун AACS у мишей in vivo знизив рівень холестерину в сироватці крові (Hasegawa et al., 2012c). SREBP-2012, головний регулятор транскрипції біосинтезу холестерину, і рецептор, активований проліфератором пероксисом (PPAR)-? є активаторами транскрипції AACS і регулюють її транскрипцію під час розвитку нейритів і в печінці (Aguilo et al., 2; Hasegawa et al., 2010c). Взято разом, метаболізм цитоплазматичних кетонових тіл може бути важливим у певних станах або природних історіях захворювань, але недостатній для утилізації кетонових тіл, отриманих з печінки, оскільки масивна гіперкетонемія виникає в умовах селективного порушення первинної окислювальної долі через втрату функціональних мутацій. до SCOT (Berry et al., 2012; Cotter et al., 2001).
Регулювання HMGCS2 і SCOT/OXCT1
Розбіжність мітохондрій від гена, що кодує цитозольний HMGCS, відбулася на ранніх етапах еволюції хребетних через необхідність підтримки печінкового кетогенезу у видів з більш високим співвідношенням маси мозку до тіла (Boukaftane et al., 1994; Cunnane and Crawford, 2003). Природні мутації HMGCS2 з втратою функції у людей викликають напади гіпокетотичної гіпоглікемії (Pitt et al., 2015; Thompson et al., 1997). Надійна експресія HMGCS2 обмежена гепатоцитами та епітелієм товстої кишки, а її експресія та ферментативна активність координуються за допомогою різноманітних механізмів (Mascaro et al., 1995; McGarry and Foster, 1980; Robinson and Williamson, 1980). Хоча повний спектр фізіологічних станів, які впливають на HMGCS2, потребує подальшого з’ясування, його експресія та/або активність регулюються протягом раннього постнатального періоду, старіння, діабету, голодування або вживання кетогенної дієти (Balasse and Fery, 1989; Cahill GF Jr, 2006). ; Girard et al., 1992; Hegardt, 1999; Satapati et al., 2012; Sengupta et al., 2010). У плода метилювання 5� фланкуючої області гена Hmgcs2 обернено корелює з його транскрипцією і частково змінюється після народження (Arias et al., 1995; Ayte et al., 1993; Ehara et al., 2015; Ferre et al. ., 1983). Аналогічно, печінковий Bdh1 демонструє модель експресії розвитку, яка збільшується від народження до відлучення, а також індукується кетогенною дієтою залежно від фактора росту фібробластів (FGF)-21 (Badman et al., 2007; Zhang et al., 1989 ). Кетогенез у ссавців дуже чутливий як до інсуліну, так і до глюкагону, пригнічується і стимулюється відповідно (McGarry and Foster, 1977). Інсулін пригнічує ліполіз жирової тканини, таким чином позбавляючи кетогенез його субстрату, тоді як глюкагон збільшує кетогенний потік через прямий вплив на печінку (Hegardt, 1999). Транскрипцію Hmgcs2 стимулює транскрипційний фактор FOXA2, який інгібується інсулін-фосфатидилінозитол-3-кіназою/Akt і індукується передачі сигналів глюкагон-цАМФ-p300 (Arias et al., 1995; Hegardt, 1999; Quant, 1990). , 1993; Thumelin et al., 2013; von Meyenn et al., 2004; Wolfrum et al., 2003; Wolfrum et al., XNUMX). PPAR? (Rodriguez et al., 1994) разом зі своєю мішенню FGF21 (Badman et al., 2007) також індукує транскрипцію Hmgcs2 в печінці під час голодування або застосування кетогенної дієти (Badman et al., 2007; Inagaki et al., 2007). ). Індукція PPAR? може відбутися до переходу від фізіології плода до новонародженого, тоді як активація FGF21 може сприяти активації в ранньому неонатальному періоді через ?OHB-опосередковане інгібування гістондеацетилази (HDAC)-3 (Rando et al., 2016). mTORC1 (мішень комплексу рапаміцину 1 у ссавців) залежить від інгібування PPAR? транскрипційна активність також є ключовим регулятором експресії гена Hmgcs2 (Sengupta et al., 2010), а PER2 печінки, головний циркадний осцилятор, опосередковано регулює експресію Hmgcs2 (Chavan et al., 2016). Останні спостереження вказують на те, що спричинений позапечінковою пухлиною інтерлейкін-6 погіршує кетогенез через PPAR? придушення (Flint et al., 2016).
Активність ферменту HMGCS2 регулюється кількома PTM. Фосфорилювання серину HMGCS2 посилило його активність in vitro (Grimsrud et al., 2012). Активність HMGCS2 алостерично інгібується сукцинилуванням сукциніл-КоА та залишків лізину (Arias et al., 1995; Hegardt, 1999; Lowe and Tubbs, 1985; Quant et al., 1990; Rardin et al., 2013; 1975; Тумелін та ін., 1993). Сукцинилування залишків лізину HMGCS2, HMGCL та BDH1 в мітохондріях печінки є мішенню для NAD+-залежної деацилази сиртуїну 5 (SIRT5) (Rardin et al., 2013). Активність HMGCS2 також посилюється деацетилюванням лізину SIRT3, і можливо, що перехресні зв’язки між ацетилюванням та сукцинилуванням регулюють активність HMGCS2 (Rardin et al., 2013; Shimazu et al., 2013). Незважаючи на здатність цих PTM регулювати HMGCS2 Km і Vmax, коливання цих PTM ще не були ретельно нанесені на карту і не були підтверджені як механістичні драйвери кетогенезу in vivo.
SCOT експресується у всіх клітинах ссавців, які містять мітохондрії, за винятком клітин гепатоцитів. Важливість активності SCOT і кетолізу була продемонстрована у мишей SCOT-KO, які демонстрували рівномірну летальність через гіперкетонемічну гіпоглікемію протягом 48 годин після народження (Cotter et al., 2011). Тканинно-специфічна втрата SCOT в нейронах або скелетних міоцитах викликає метаболічні порушення під час голодування, але не є смертельною (Cotter et al., 2013b). У людей дефіцит SCOT на ранньому етапі життя проявляється важким кетоацидозом, що викликає летаргію, блювоту та кому (Berry et al., 2001; Fukao et al., 2000; Kassovska-Bratinova et al., 1996; Niezen-Koning et al. , 1997; Saudubray et al., 1987; Snyderman et al., 1998; Tildon and Cornblath, 1972). На клітинному рівні відомо відносно мало про регулятори експресії гена SCOT і білка. Експресія мРНК Oxct1 і білка SCOT і активність зменшуються в кетотичних станах, можливо, через PPAR-залежні механізми (Fenselau and Wallis, 1974; Fenselau and Wallis, 1976; Grinblat et al., 1986; Okuda et al., 1991; Turko et al. ., 2001; Wentz та ін., 2010). При діабетичному кетоацидозі невідповідність між печінковим кетогенезом і позапечінковим окисленням посилюється через порушення активності SCOT. Надмірна експресія інсулінонезалежного транспортера глюкози (GLUT1/SLC2A1) в кардіоміоцитах також пригнічує експресію гена Oxct1 і пригнічує термінальне окислення кетонів у некетотичному стані (Yan et al., 2009). У печінці кількість мРНК Oxct1 пригнічується мікроРНК-122 і метилюванням гістонів H3K27me3, що є очевидним під час переходу від фетального до неонатального періоду (Thorrez et al., 2011). Однак придушення печінкової експресії Oxct1 в постнатальному періоді в першу чергу пояснюється евакуацією Oxct1-експресуючих гемопоетичних попередників з печінки, а не втратою раніше існуючої експресії Oxct1 в термінально диференційованих гепатоцитах. Насправді експресія мРНК Oxct1 і білка SCOT в диференційованих гепатоцитах надзвичайно низька (Orii et al., 2008).
SCOT також регулюється PTM. Фермент гіперацетильований в мозку мишей SIRT3 KO, які також демонструють знижене залежне від AcAc виробництво ацетил-КоА (Dittenhafer-Reed et al., 2015). Неферментативне нітрування залишків тирозину SCOT також послаблює його активність, про що повідомлялося в серцях різних моделей діабетичних мишей (Marcondes et al., 2001; Turko et al., 2001; Wang et al., 2010a). Навпаки, нітрування залишків триптофану збільшує активність SCOT (Br�g�re et al., 2010; Rebrin et al., 2007). Молекулярні механізми специфічного для залишків нітрування або денітрування, призначені для модуляції активності SCOT, можуть існувати і вимагати з’ясування.
Суперечки в позапечінковому кетогенезі
У ссавців первинним кетогенним органом є печінка, і лише гепатоцити та епітеліальні клітини кишечника рясно експресують мітохондріальну ізоформу HMGCS2 (Cotter et al., 2013a; Cotter et al., 2014; McGarry and Foster, 1980; Robinson1980 і Williamson). . Анаеробна бактеріальна ферментація складних полісахаридів дає бутират, який поглинається колоноцитами у ссавців для кінцевого окислення або кетогенезу (Cherbuy et al., 1995), що може відігравати роль у диференціації колоноцитів (Wang et al., 2016). За винятком епітеліальних клітин і гепатоцитів кишечника, HMGCS2 майже відсутній майже у всіх інших клітинах ссавців, але перспектива позапечінкового кетогенезу була підвищена в пухлинних клітинах, астроцитах центральної нервової системи, нирках, підшлунковій залозі. клітини, пігментний епітелій сітківки (RPE) і навіть у скелетних м’язах (Adijanto et al., 2014; Avogaro et al., 1992; El Azzouny et al., 2016; Grabacka et al., 2016; Kang et al., 2015 ; Le Foll et al., 2014; Nonaka et al., 2016; Takagi et al., 2016a; Thevenet et al., 2016; Zhang et al., 2011). Ектопічний HMGCS2 спостерігався в тканинах, яким не вистачає чистої кетогенної здатності (Cook et al., 2016; Wentz et al., 2010), а HMGCS2 проявляє проспективну незалежну від кетогенезу «підготовку» активність, у тому числі всередині клітинного ядра (Chen et al. , 2016; Костюк та ін., 2010; Меертенс та ін., 1998).
Будь-яка позапечінкова тканина, яка окислює кетонові тіла, також може накопичувати кетонові тіла за допомогою незалежних механізмів HMGCS2 (рис. 2A). Однак немає позапечінкової тканини, в якій стабільна концентрація кетонових тіл перевищує концентрацію в циркуляції (Cotter et al., 2011; Cotter et al., 2013b; Harrison and Long, 1940), що підкреслює, що кетонові тіла транспортуються вниз градієнт концентрації через MCT1/2-залежні механізми. Один з механізмів очевидного позапечінкового кетогенезу може насправді відображати відносне порушення окислення кетонів. Додаткові потенційні пояснення належать до сфери утворення кетонових тіл. По-перше, кетогенез de novo може відбуватися через оборотну ферментативну активність тіолази та SCOT (Weidemann and Krebs, 1969). Коли концентрація ацетил-КоА відносно висока, реакції, які зазвичай відповідають за окислення AcAc, відбуваються у зворотному напрямку (GOLDMAN, 1954). Другий механізм виникає, коли проміжні продукти, отримані від ?-окислення, накопичуються через вузьке місце циклу TCA, AcAc-CoA перетворюється на l-?OHB-CoA за допомогою реакції, що каталізується мітохондріальною 3-гідроксиацил-КоА-дегідрогеназою, а також 3-гідроксибутирилом. КоА деацилаза до l-?OHB, яку неможливо відрізнити за допомогою мас-спектрометрії або резонансної спектроскопії від фізіологічного енантіомеру d-?OHB (Reed and Ozand, 1980). l-?OHB можна хроматографічно або ферментативно відрізнити від d-?OHB, і він присутній у позапечінкових тканинах, але не в печінці чи крові (Hsu et al., 2011). Печінковий кетогенез утворює лише d-?OHB, єдиний енантіомер, який є субстратом BDH (Ito et al., 1984; Lincoln et al., 1987; Reed and Ozand, 1980; Scofield et al., 1982; Scofield et al., 1982). Третій HMGCS2-незалежний механізм генерує d-?OHB через катаболізм амінокислот, зокрема лейцину та лізину. Четвертий механізм є очевидним лише тому, що він пов’язаний з артефактом мічення, тому його називають псевдокетогенезом. Це явище пояснюється оборотністю реакцій SCOT і тіолази і може викликати переоцінку обміну кетонових тіл через ізотопне розведення індикатора кетонових тіл у позапечінковій тканині (Des Rosiers et al., 1990; Fink et al., 1988). . Тим не менш, псевдокетогенез може бути незначним у більшості контекстів (Bailey et al., 1990; Keller et al., 1978). Схема (рис. 2A) вказує на корисний підхід, який слід застосувати, розглядаючи підвищену концентрацію кетонів у стабільному стані тканини.
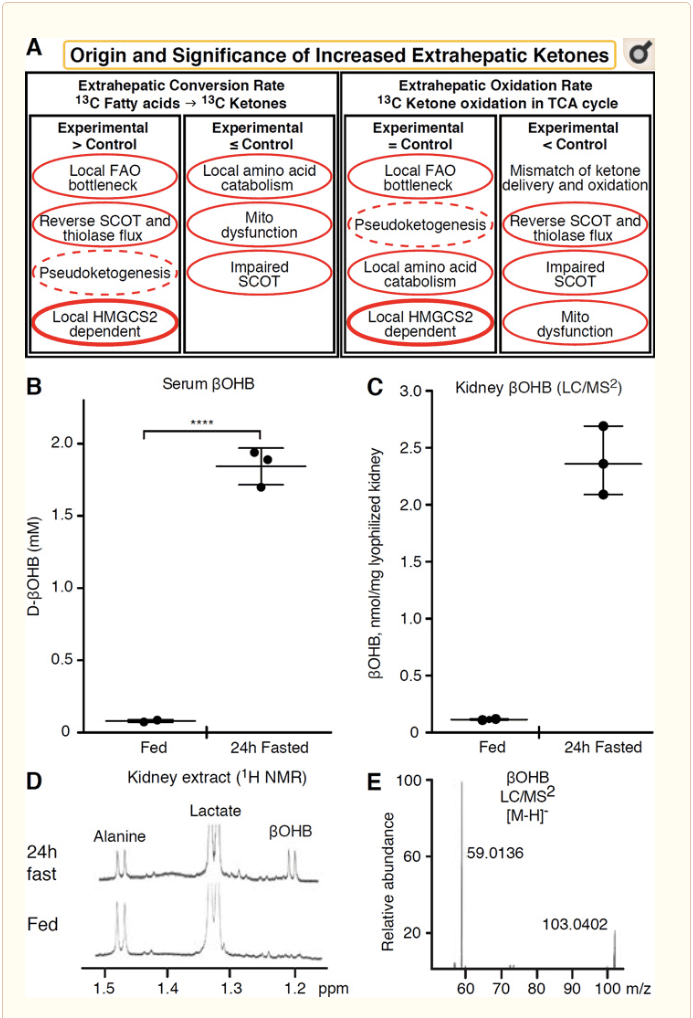

� Нирки нещодавно приділяли увагу як потенційно кетогенний орган. У переважній більшості штатів нирки є чистим споживачем кетонових тіл, отриманих з печінки, виділяють або реабсорбують кетонові тіла з кровотоку, а нирка, як правило, не є чистим генератором або концентратором кетонових тіл (Robinson and Williamson, 1980). Автори класичного дослідження дійшли висновку, що мінімальний нирковий кетогенез, кількісно визначений у штучній експериментальній системі, не має фізіологічного значення (Weidemann and Krebs, 1969). Нещодавно на моделях мишей з цукровим діабетом та дефіцитом аутофагії було зроблено висновок про нирковий кетогенез, але більш імовірно, що багатоорганні зрушення в метаболічному гомеостазі змінюють інтегративний кетоновий метаболізм через введення в різні органи (Takagi et al., 2016a; Takagi et al., 2016b; Zhang et al., 2011). В одній нещодавній публікації було запропоновано нирковий кетогенез як захисний механізм проти ішемічно-реперфузійного ураження нирок (Tran et al., 2016). Повідомлялося про абсолютну рівноважну концентрацію ?OHB з екстрактів ниркової тканини мишей на рівні ~4 мМ. Щоб перевірити, чи це було спроможним, ми кількісно визначили концентрації ?OHB в ниркових екстрактах мишей, які годували та голодували протягом 12 годин. Концентрація ?OHB у сироватці зросла від ~24 мМ до 100 мМ при 2-годинному голодуванні (рис. 24В), у той час як концентрація ?OHB у нирках у рівноважному стані становить приблизно 2 мкМ у стані нагодування і лише 100 мМ у стані 1-годинного голодування (рис. 24C�E), спостереження, які узгоджуються з кількісно визначеними концентраціями понад 2 років тому (Hems and Brosnan, 45). Залишається можливим, що в кетозних станах кетонові тіла, отримані з печінки, можуть бути ренопротекторними, але докази ниркового кетогенезу потребують додаткового обґрунтування. Переконливі докази, що підтверджують справжній позапечінковий кетогенез, були представлені в RPE (Adijanto et al., 1970). Було запропоновано, що ця інтригуюча метаболічна трансформація потенційно дозволить кетонам, отриманим з RPE, надходити до фоторецепторних клітин або клітин глії Меллера, що може сприяти регенерації зовнішнього сегмента фоторецептора.
OHB як посередник сигналізації
Хоча вони енергетично багаті, кетонові тіла виконують провокаційні «неканонічні» сигнальні ролі в клітинному гомеостазі (рис. 3) (Newman and Verdin, 2014; Rojas-Morales et al., 2016). Наприклад, ?OHB інгібує HDAC класу I, що посилює ацетилювання гістонів і, таким чином, індукує експресію генів, які знижують окислювальний стрес (Shimazu et al., 2013). Сам ?OHB є ковалентним модифікатором гістонів на залишки лізину в печінці діабетичних мишей натщесерце або індукованих стрептозотоцином (Xie et al., 2016) (також див. нижче, Інтеграція метаболізму кетонових тіл, посттрансляційної модифікації та фізіології клітин та Кетонові тіла, окислювальний стрес і нейропротекция).
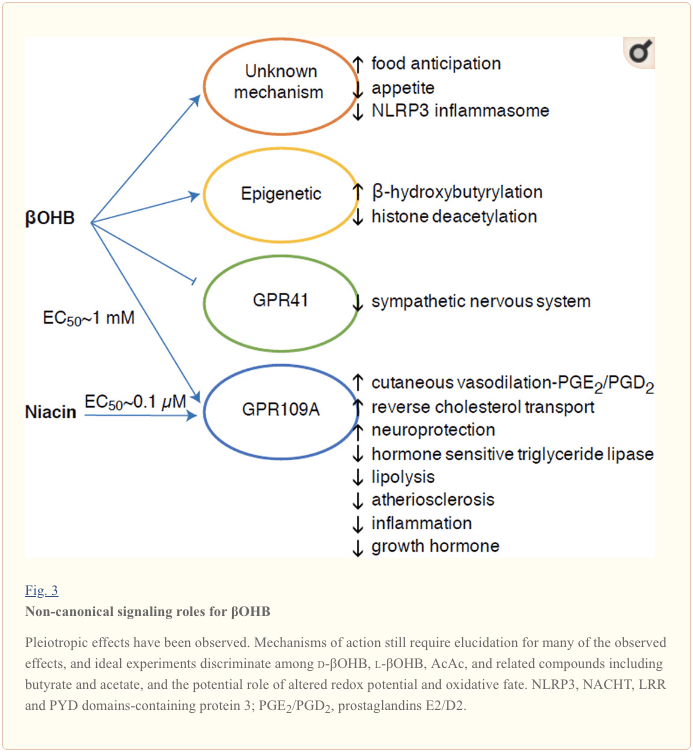
?OHB також є ефектором через рецептори, пов'язані з G-білком. Завдяки незрозумілим молекулярним механізмам він пригнічує активність симпатичної нервової системи та зменшує загальні витрати енергії та частоту серцевих скорочень, пригнічуючи передачу сигналів коротколанцюгових жирних кислот через рецептор, пов’язаний з G-білком 41 (GPR41) (Kimura et al., 2011). Один з найбільш вивчених сигнальних ефектів ?OHB протікає через GPR109A (також відомий як HCAR2), член підродини GPCR гідрокарбонових кислот, що експресується в жировій тканині (білої та коричневої) (Tunaru et al., 2003), і в імунні клітини (Ahmed et al., 2009). ?OHB є єдиним відомим ендогенним лігандом рецептора GPR109A (EC50 ~770 мкМ), активованим d-?OHB, l-?OHB і бутиратом, але не AcAc (Taggart et al., 2005). Високий поріг концентрації для активації GPR109A досягається шляхом дотримання кетогенної дієти, голодування або під час кетоацидозу, що призводить до пригнічення ліполізу жирової тканини. Антиліполітичний ефект GPR109A протікає через інгібування аденілілциклази та зниження цАМФ, інгібуючи чутливу до гормонів тригліцерид-ліпазу (Ahmed et al., 2009; Tunaru et al., 2003). Це створює петлю негативного зворотного зв’язку, в якій кетоз гальмує кетогенез, зменшуючи вивільнення неетерифікованих жирних кислот з адипоцитів (Ahmed et al., 2009; Taggart et al., 2005), ефект, який можна збалансувати симпатичний потяг, який стимулює ліполіз. Ніацин (вітамін B3, нікотинова кислота) є потужним (EC50 ~ 0.1 мкМ) лігандом для GRP109A, ефективно використовуваним протягом десятиліть для лікування дисліпідемій (Benyo et al., 2005; Benyo et al., 2006; Fabbrini et al.;, 2010; Лукасова та ін., 2011; Тунару та ін., 2003). Хоча ніацин посилює зворотний транспорт холестерину в макрофагах і зменшує атеросклеротичні ураження (Lukasova et al., 2011), вплив ?OHB на атеросклеротичні ураження залишається невідомим. Хоча рецептор GPR109A виконує захисну роль, і існують інтригуючі зв’язки між використанням кетогенної дієти при інсульті та нейродегенеративних захворюваннях (Fu et al., 2015; Rahman et al., 2014), захисна роль ?OHB через GPR109A не була продемонстрована in vivo .
Нарешті, ?OHB може впливати на апетит і ситість. Метааналіз досліджень, які вимірювали вплив кетогенних дієт і дієт з дуже низьким вмістом енергії, показав, що учасники, які споживають ці дієти, демонструють вищу ситість порівняно з контрольними дієтами (Gibson et al., 2015). Однак правдоподібним поясненням цього ефекту є додаткові метаболічні або гормональні елементи, які можуть модулювати апетит. Наприклад, миші, які перебували на кетогенній дієті для гризунів, демонстрували підвищені витрати енергії порівняно з мишами, які харчувалися контрольною їжею, незважаючи на подібне споживання калорій, а циркулюючий лептин або гени пептидів, що регулюють харчову поведінку, не змінювалися (Kennedy et al., 2007). Серед запропонованих механізмів, які припускають придушення апетиту за допомогою ?OHB, є як передача сигналів, так і окислення (Laeger et al., 2010). Дослідження специфічної для гепатоцитів делеції гена циркадного ритму (Per2) і імунопреципітації хроматину показали, що PER2 безпосередньо активує ген Cpt1a і опосередковано регулює Hmgcs2, що призводить до порушення кетозу у мишей з нокаутом Per2 (Chavan et al., Chavan et al.). У цих мишей спостерігалося порушення очікування їжі, яке було частково відновлено системним введенням ?OHB. Потрібні подальші дослідження, щоб підтвердити центральну нервову систему як пряму ?OHB-мішень, і чи потрібне окислення кетонів для спостережуваних ефектів, чи задіяний інший сигнальний механізм. Інші дослідники посилалися на можливість локального кетогенезу, отриманого з астроцитів у вентромедіальному гіпоталамусі, як на регулятор споживання їжі, але ці попередні спостереження також будуть корисними від генетичних оцінок та оцінок на основі потоків (Le Foll et al., 2016). Зв'язок між кетозом і нестачею поживних речовин залишається цікавим, оскільки голод і насичення є важливими елементами невдалих спроб схуднути.
Інтеграція метаболізму кетонового тіла, посттрансляційної модифікації та фізіології клітини
Кетонові тіла сприяють утворенню розділених пулів ацетил-КоА, ключового проміжного продукту, який відіграє важливу роль у клітинному метаболізмі (Pietrocola et al., 2015). Одна з функцій ацетил-КоА полягає в тому, щоб служити субстратом для ацетилювання, ковалентної модифікації гістонів, що каталізується ферментами (Choudhary et al., 2014; Dutta et al., 2016; Fan et al., 2015; Menzies et al., 2016 ). Велика кількість динамічно ацетильованих мітохондріальних білків, багато з яких можуть виникати за допомогою неферментативних механізмів, також з'явилася в результаті обчислювальних протеомічних досліджень (Dittenhafer-Reed et al., 2015; Hebert et al., 2013; Rardin et al., 2013 ; Shimazu et al., 2010). Лізиндеацетилази використовують кофактор цинку (наприклад, нуклеоцитозольні HDAC) або NAD+ як сусубстрат (сиртуїни, SIRT) (Choudhary et al., 2014; Menzies et al., 2016). Ацетилпротеом служить одночасно датчиком і ефектором загального клітинного пулу ацетил-КоА, оскільки фізіологічні та генетичні маніпуляції призводять до неферментативних глобальних варіацій ацетилювання (Weinert et al., 2014). Оскільки внутрішньоклітинні метаболіти служать модуляторами ацетилювання залишків лізину, важливо враховувати роль кетонових тіл, чисельність яких дуже динамічна.
?OHB є епігенетичним модифікатором принаймні за двома механізмами. Підвищені рівні ?OHB, викликані голодуванням, обмеженням калорій, прямим прийомом або тривалими фізичними вправами провокують інгібування HDAC або активацію гістонацетилтрансферази (Marosi et al., 2016; Sleiman et al., 2016) або окислювальний стрес (Shimazu et al., 2013) 3. . Інгібування ?OHB HDAC2016 може регулювати метаболічну фізіологію новонароджених (Rando et al., 2016). Незалежно, сам ?OHB безпосередньо модифікує залишки лізину гістонів (Xie et al., XNUMX). Тривале голодування або діабетичний кетоацидоз, викликаний стептозотоцином, посилює ?-гідроксибутирилювання гістонів. Хоча кількість сайтів α-гідроксибутирилування та ацетилювання лізину була порівнянною, спостерігалося стехіометричне β-гідроксибутирилування гістонів, ніж ацетилювання. На окремі гени вплинуло α-гідроксибутирилування гістону лізину проти ацетилювання або метилювання, що свідчить про різні клітинні функції. Невідомо, чи є ?-гідроксибутирилювання спонтанним чи ферментативним, але розширює діапазон механізмів за рахунок кетонових тіл, які динамічно впливають на транскрипцію.
Основні події перепрограмування клітин під час обмеження калорій і нестачі поживних речовин можуть бути опосередковані в SIRT3- та SIRT5-залежному мітохондріальному деацетилюванні та десукцинилуванні, відповідно, регулюючи кетогенні та кетолітичні білки на посттрансляційному рівні в печінці та позапечінкових тканинах (ReDittenhafer al. 2015; Hebert et al., 2013; Rardin et al., 2013; Shimazu et al., 2010). Незважаючи на те, що стехіометричне порівняння зайнятих ділянок не обов’язково безпосередньо пов’язане зі зрушеннями метаболічного потоку, ацетилювання мітохондрій є динамічним і може обумовлюватися концентрацією ацетил-КоА або мітохондріальним pH, а не ферментативними ацетилтрансферазами (Wagner and Payne, 2013). Те, що SIRT3 і SIRT5 модулюють активність ферментів, що метаболізують кетонові тіла, викликає питання про взаємну роль кетонів у формуванні ацетилпротеома, сукцинілпротеома та інших динамічних клітинних мішеней. Дійсно, оскільки варіації кетогенезу відображають концентрації NAD+, виробництво та кількість кетону можуть регулювати активність сиртуїну, впливаючи таким чином на загальні пули ацетил-КоА/сукциніл-КоА, ацилпротеом і, таким чином, фізіологію мітохондрій і клітин. ?-гідроксибутирилювання залишків ферменту лізину може додати ще один шар до клітинного перепрограмування. У позапечінкових тканинах окислення кетонових тіл може стимулювати аналогічні зміни гомеостазу клітин. У той час як компартментація пулів ацетил-КоА дуже регулюється і координує широкий спектр клітинних змін, здатність кетонових тіл безпосередньо формувати концентрацію ацетил-КоА в мітохондріях і цитоплазмі потребує з’ясування (Chen et al., 2012; Corbet et al., 2016; Поуговкіна та ін., 2014; Швер та ін., 2009; Wellen and Thompson, 2012). Оскільки концентрації ацетил-КоА жорстко регулюються, а ацетил-КоА є непроникним для мембрани, важливо враховувати механізми, що координують гомеостаз ацетил-КоА, включаючи швидкість виробництва та кінцевого окислення в циклі TCA, перетворення в кетонові тіла, мітохондріальні відтік через карнітин-ацетилтрансферазу (CrAT) або експорт ацетил-КоА в цитозоль після перетворення в цитрат і вивільнення за допомогою АТФ-цитрат-ліази (ACLY). Ключова роль цих останніх механізмів у клітинному ацетилпротеомі та гомеостазі вимагає відповідного розуміння ролі кетогенезу та окислення кетонів (Das et al., 2015; McDonnell et al., 2016; Moussaieff et al., 2015; Overmyer et al., 2015; Seiler et al., 2014; Seiler et al., 2015; Wellen et al., 2009; Wellen and Thompson, 2012). Для визначення цілей та результатів знадобляться конвергентні технології в метаболоміці та ацилпротеоміці в умовах генетично маніпульованих моделей.
Проти- та прозапальні реакції на кетонові тіла
Кетоз і кетонові тіла модулюють запалення і функцію імунних клітин, але були запропоновані різноманітні і навіть невідповідні механізми. Тривала нестача поживних речовин зменшує запалення (Youm et al., 2015), але хронічний кетоз діабету 1 типу є прозапальним станом (Jain et al., 2002; Kanikarla-Marie and Jain, 2015; Kurepa et al., 2012). ). Сигнальні ролі для ?OHB у запаленні з’являються на основі механізмів, оскільки багато клітин імунної системи, включаючи макрофаги або моноцити, рясно експресують GPR109A. Хоча ?OHB має переважно протизапальну відповідь (Fu et al., 2014; Gambhir et al., 2012; Rahman et al., 2014; Youm et al., 2015), високі концентрації кетонових тіл, зокрема AcAc, можуть викликати прозапальну відповідь (Jain et al., 2002; Kanikarla-Marie and Jain, 2015; Kurepa et al., 2012).
Було розглянуто протизапальну роль лігандів GPR109A при атеросклерозі, ожирінні, запальних захворюваннях кишечника, неврологічних захворюваннях та раку (Graff et al., 2016). Експресія GPR109A посилюється в клітинах RPE моделей діабету, пацієнтів з діабетом (Gambhir et al., 2012) і в мікроглії під час нейродегенерації (Fu et al., 2014). Протизапальні ефекти ?OHB посилюються через надмірну експресію GPR109A в клітинах RPE і скасовуються фармакологічним інгібуванням або генетичним нокаутом GPR109A (Gambhir et al., 2012). ?OHB і екзогенна нікотинова кислота (Taggart et al., 2005), обидва надають протизапальну дію на TNF? або запалення, спричинене LPS шляхом зниження рівня прозапальних білків (iNOS, COX-2) або секретованих цитокінів (TNF?, IL-1?, IL-6, CCL2/MCP-1), частково через інгібування NF -?B транслокація (Fu et al., 2014; Gambhir et al., 2012). ?OHB зменшує ER-стрес і інфламасому NLRP3, активуючи відповідь на антиоксидантний стрес (Bae et al., 2016; Youm et al., 2015). Однак при нейродегенеративному запаленні GPR109A-залежний ?OHB-опосередкований захист не включає медіатори запалення, такі як передача сигналів MAPK (наприклад, ERK, JNK, p38) (Fu et al., 2014), але може знадобитися ЦОГ-1-залежний PGD2 виробництво (Rahman et al., 2014). Цікаво, що макрофаг GPR109A необхідний для прояву нейропротекторного ефекту в моделі ішемічного інсульту (Rahman et al., 2014), але здатність ?OHB пригнічувати запалення NLRP3 у макрофагах, отриманих з кісткового мозку, не залежить від GPR109A та ін. ., 2015). Хоча більшість досліджень пов’язують ?OHB з протизапальною дією, ?OHB може бути прозапальним і підвищувати маркери перекисного окислення ліпідів у гепатоцитах теляти (Shi et al., 2014). Таким чином, протизапальні ефекти ?OHB можуть залежати від типу клітин, концентрації ?OHB, тривалості впливу та наявності чи відсутності співмодуляторів.
На відміну від ?OHB, AcAc може активувати прозапальну передачу сигналів. Підвищений AcAc, особливо при високій концентрації глюкози, посилює пошкодження ендотеліальних клітин через механізм, що залежить від НАДФН-оксидази/оксидативного стресу (Kanikarla-Marie and Jain, 2015). Високі концентрації AcAc у пуповині матерів з цукровим діабетом корелювали з вищою швидкістю окислення білка та концентрацією MCP-1 (Kurepa et al., 2012). Високий AcAc у пацієнтів з цукровим діабетом корелював з TNF? експресія (Jain et al., 2002) і AcAc, але не ?OHB, індукували експресію TNF?, MCP-1, накопичення АФК та знижували рівень цАМФ в клітинах моноцитів людини U937 (Jain et al., 2002; Kurepa et al. ., 2012).
Сигнальні явища, залежні від кетонових тіл, часто викликаються лише при високій концентрації кетонових тіл (> 5 мМ), а у випадку багатьох досліджень, які пов’язують кетони з про- або протизапальними ефектами, через незрозумілі механізми. Крім того, через суперечливий вплив ?OHB проти AcAc на запалення та здатність співвідношення AcAc/?OHB впливати на мітохондріальний окислювально-відновний потенціал, найкращі експерименти, що оцінюють роль кетонових тіл на клітинні фенотипи, порівнюють ефекти AcAc і ? OHB у різних співвідношеннях і в різних кумулятивних концентраціях [наприклад, (Saito et al., 2016)]. Нарешті, AcAc можна придбати в комерційних цілях лише у вигляді літієвої солі або у вигляді етилового ефіру, який вимагає гідролізу основи перед використанням. Катіон літію незалежно індукує каскади передачі сигналу (Manji et al., 1995), а аніон AcAc є лабільним. Нарешті, дослідження з використанням рацемічного d/l-?OHB можуть бути заплутаними, оскільки лише стереоізомер d-?OHB може бути окислений до AcAc, але d-?OHB і l-?OHB можуть кожен сигналізувати через GPR109A, інгібувати запалення NLRP3, і служать ліпогенними субстратами.
Кетонові тіла, окислювальний стрес і нейропротекція
Окислювальний стрес, як правило, визначається як стан, в якому АФК представлені в надлишку через надмірну продукцію та/або порушення елімінації. Ролі кетонових тіл, що пом’якшують антиоксидантний та окислювальний стрес, широко описані як in vitro, так і in vivo, особливо в контексті нейропротекції. Оскільки більшість нейронів не ефективно виробляють високоенергетичні фосфати з жирних кислот, але окислюють кетонові тіла, коли вуглеводів не вистачає, нейропротекторний ефект кетонових тіл особливо важливий (Cahill GF Jr, 2006; Edmond et al., 1987; Yang та ін., 1987). У моделях окисного стресу індукція BDH1 і пригнічення SCOT припускають, що метаболізм кетонових тіл можна перепрограмувати для підтримки різноманітних клітинних сигналів, окислювально-відновного потенціалу або метаболічних потреб (Nagao et al., 2016; Tieu et al., 2003).
Кетонові тіла знижують ступінь пошкодження клітин, пошкодження, смерть та зниження апоптозу в нейронах і кардіоміоцитах (Haces et al., 2008; Maalouf et al., 2007; Nagao et al., 2016; Tieu et al., 2003). Викликані механізми різноманітні і не завжди лінійно пов’язані з концентрацією. Низькі мілімолярні концентрації (d або l)-?OHB поглинають АФК (гідроксильний аніон), тоді як AcAc поглинає численні види АФК, але лише в концентраціях, які перевищують фізіологічний діапазон (IC50 20 мМ) (Haces et al., 67) . І навпаки, сприятливий вплив на окислювально-відновний потенціал ланцюга транспорту електронів є механізмом, який зазвичай пов’язаний з d-?OHB. Хоча всі три кетонових тіла (d/l-?OHB і AcAc) зменшували загибель нейронних клітин і накопичення АФК, викликане хімічним пригніченням гліколізу, лише d-?OHB і AcAc запобігали зниженню АТФ нейронів. І навпаки, у гіпоглікемічній моделі in vivo (d або l)-?OHB, але не AcAc запобігали перекисному окисненню ліпідів гіпокампу (Haces et al., 2008; Maalouf et al., 2008; Marosi et al., 2007; Murphy, 2016 ; Tieu та ін., 2009). Дослідження in vivo на мишах, яких годували кетогенною дієтою (2003% ккал жиру і 87% білка), показали нейроанатомічні варіації антиоксидантної здатності (Ziegler et al., 13), де найбільш глибокі зміни спостерігалися в гіпокампі з підвищенням глутатіонпероксидази та загального антиоксидантні можливості.
Кетогенна дієта, кетонові ефіри (також див. Терапевтичне використання кетогенної дієти та екзогенних кетонових тіл) або введення ?OHB надають нейропротекцію на моделях ішемічного інсульту (Rahman et al., 2014); хвороба Паркінсона (Tieu et al., 2003); напад кисневої токсичності центральної нервової системи (D'Agostino et al., 2013); епілептичні спазми (Yum et al., 2015); мітохондріальна енцефаломіопатія, синдром лактоацидозу та інсультоподібних (MELAS) епізодів (Frey et al., 2016) і хвороби Альцгеймера (Cunnane and Crawford, 2003; Yin et al., 2016). І навпаки, нещодавня доповідь продемонструвала гістопатологічні докази нейродегенеративного прогресування за допомогою кетогенної дієти на моделі аномальної репарації мітохондріальної ДНК трансгенної миші, незважаючи на збільшення мітохондріального біогенезу та антиоксидантних сигнатур (Lauritzen et al., 2016). Інші суперечливі повідомлення свідчать про те, що вплив високих концентрацій кетонових тіл викликає окислювальний стрес. Високі дози ?OHB або AcAc викликали секрецію оксиду азоту, перекисне окислення ліпідів, знижену експресію SOD, глутатіонпероксидази і каталази в гепатоцитах теляти, тоді як у гепатоцитах щурів індукція шляху MAPK приписується AcAc, але не ?OHB (Abdelmegeed et al. ; Ши та ін., 2004; Ши та ін., 2014).
У сукупності більшість звітів пов’язують ?OHB з ослабленням окислювального стресу, оскільки його введення пригнічує вироблення АФК/супероксиду, запобігає перекисному окисленню ліпідів і окислення білка, підвищує рівень антиоксидантного білка та покращує мітохондріальне дихання та виробництво АТФ (Abdelmegeed et al., 2004); Haces et al., 2008; Jain et al., 1998; Jain et al., 2002; Kanikarla-Marie and Jain, 2015; Maalouf та ін., 2007; Maalouf і Rho, 2008; Marosi та ін., 2016; Tie та ін., 2003; Yin та ін., 2016; Ziegler та ін., 2003). Хоча AcAc був більш прямим, ніж ?OHB, пов’язаний з індукцією окисного стресу, ці ефекти не завжди легко відокремити від потенційних прозапальних реакцій (Jain et al., 2002; Kanikarla-Marie and Jain, 2015; Kanikarla-Marie та Джейн, 2016). Крім того, важливо враховувати, що очевидна антиоксидантна користь, яку надають плейотропні кетогенні дієти, не може бути перетворена самими кетоновими тілами, а нейропротекція, яка надається кетоновими тілами, не може бути повністю пов’язана з окислювальним стресом. Наприклад, під час депривації глюкози, в моделі депривації глюкози в нейронах кори, ?OHB стимулював аутофагічний потік і запобігав накопиченню аутофагосом, що було пов’язано зі зниженням загибелі нейронів (Camberos-Luna et al., 2016). d-?OHB також індукує канонічні антиоксидантні білки FOXO3a, SOD, MnSOD і каталазу, проспективно через інгібування HDAC (Nagao et al., 2016; Shimazu et al., 2013).
Неалкогольна жирова хвороба печінки (НАЖХП) і метаболізм кетонового тіла
НАЖХП, асоційована з ожирінням, і неалкогольний стеатогепатит (НАСГ) є найпоширенішими причинами захворювань печінки в західних країнах (Rinella and Sanyal, 2016), а печінкова недостатність, спричинена НАСГ, є однією з найпоширеніших причин для трансплантації печінки. У той час як надлишок триацилгліцеролів у гепатоцитах >5% маси печінки (NAFL) сам по собі не викликає дегенеративної функції печінки, прогресування НАЖХП у людей корелює із системною резистентністю до інсуліну та підвищеним ризиком діабету 2 типу та може сприяти патогенезу захворювання. серцево-судинні захворювання та хронічні захворювання нирок (Fabbrini et al., 2009; Targher et al., 2010; Targher and Byrne, 2013). Патогенні механізми НАЖХП і НАСГ вивчені не повністю, але включають порушення метаболізму гепатоцитів, аутофагію гепатоцитів і стрес ендоплазматичного ретикулума, функцію імунних клітин печінки, запалення жирової тканини та системні медіатори запалення (Fabbrini et al., 2009, Masaniu2013, 2010; ; Targher et al., 2010; Yang et al., 2012). Порушення метаболізму вуглеводів, ліпідів та амінокислот виникають у людей та модельних організмів і сприяють ожирінню, діабету та НАЖХП [огляд у (Farese et al., 2011; Lin and Accili, 2012; Newgard, 2012; Samuel and Шульман, 2013; Sun and Lazar, 2010)]. У той час як аномалії гепатоцитів у метаболізмі ліпідів цитоплазми зазвичай спостерігаються при НАЖХП (Fabbrini et al., 2016b), роль мітохондріального метаболізму, який регулює окислювальне видалення жирів, менш ясна в патогенезі НАЖХП. Аномалії мітохондріального метаболізму виникають і сприяють патогенезу НАЖХП/НАСГ (Hyotylainen et al., 2011; Serviddio et al., 2008; Serviddio et al., 2008; Wei et al., 1974). Існує загальне (Felig et al., 2010; Iozzo et al., 2015; Koliaki et al., 2015; Satapati et al., 2012; Satapati et al., 2011; Sunny et al., 2013), але не однорідне ( Koliaki and Roden, 2016; Perry et al., 2010; Rector et al., 2015) консенсус про те, що до розвитку добросовісного НАСГ окислення мітохондрій печінки і, зокрема окислення жиру, посилюється при ожирінні, системній інсулінорезистентності. і НАЖХП. Цілком імовірно, що в міру прогресування НАЖХП з’являється гетерогенність окислювальної здатності, навіть серед окремих мітохондрій, і в кінцевому підсумку окислювальна функція порушується (Koliaki et al., 2010; Rector et al., 2008; Satapati et al., 2012; Satapati et al. ., XNUMX).
Кетогенез часто використовується як проксі для окислення печінкового жиру. Порушення кетогенезу виникають у міру прогресування НАЖХП на тваринних моделях і, ймовірно, у людей. Через неповно визначені механізми гіперінсулінемія пригнічує кетогенез, що, можливо, сприяє гіпокетонемії в порівнянні з контрольною групою з худим організмом (Bergman et al., 2007; Bickerton et al., 2008; Satapati et al., 2012; Soeters et al., Sunny et al., Sunny , 2009; Vice та ін., 2011). Тим не менш, здатність концентрації циркулюючих кетонових тіл передбачати НАЖХП є суперечливою (M�nnist� et al., 2005; Sanyal et al., 2015). Надійні кількісні магнітно-резонансні спектроскопічні методи на тваринних моделях виявили збільшення швидкості обміну кетонів при помірній інсулінорезистентності, але зниження показників було очевидним при більш вираженій інсулінорезистентності (Satapati et al., 2001; Sunny et al., 2012). У людей з ожирінням із жировою печінкою швидкість кетогенезу є нормальною (Bickerton et al., 2010; Sunny et al., 2008), і, отже, швидкість кетогенезу зменшується порівняно зі збільшенням навантаження жирних кислот у гепатоцитах. Отже, ацетил-КоА, отриманий від ?-окислення, може бути спрямований на кінцеве окислення в циклі ТСА, посилюючи термінальне окислення, глюконеогенез, керований фосфоенолпіруватом через анаплероз/катаплероз, і окислювальний стрес. Ацетил-КоА також, можливо, експортується з мітохондрій у вигляді цитрату, субстрату-попередника для ліпогенезу (рис. 2011) (Satapati et al., 4; Satapati et al., 2015; Solinas et al., 2012). Хоча кетогенез стає менш чутливим до інсуліну або голодування при тривалому ожирінні (Satapati et al., 2015), основні механізми та наслідки цього залишаються неповністю зрозумілими. Останні дані вказують на те, що mTORC2012 пригнічує кетогенез таким чином, що може бути нижче за передачу сигналів інсуліну (Kucejova et al., 1), що узгоджується з спостереженнями про те, що mTORC2016 пригнічує PPAR?-опосередковану індукцію Hmgcs1 (Sengupta et al.), 2 також див. Регламент HMGCS2010 і SCOT/OXCT2).

Попередні спостереження нашої групи свідчать про несприятливі наслідки кетогенної недостатності для печінки (Cotter et al., 2014). Щоб перевірити гіпотезу про те, що порушення кетогенезу, навіть у багатих вуглеводами і, таким чином, «некетогенних» станах сприяє аномальному метаболізму глюкози та провокує стеатогепатит, ми створили мишачу модель вираженої кетогенної недостатності шляхом введення антисмислового олігонуклеї-мішені (ASO). Hmgcs2. Втрата HMGCS2 у дорослих мишей, яких годували стандартними їжею з низьким вмістом жиру, спричинила легку гіперглікемію та помітно збільшила продукцію сотень печінкових метаболітів, набір яких вказував на активацію ліпогенезу. Харчування мишей з високим вмістом жиру з недостатнім кетогенезом призводило до обширного пошкодження та запалення гепатоцитів. Ці висновки підтверджують головну гіпотезу про те, що (i) кетогенез не є пасивним шляхом переповнення, а скоріше динамічним вузлом у печінковому та інтегрованому фізіологічному гомеостазі, і (ii) заслуговує на дослідження розумне кетогенне збільшення для пом’якшення НАЖХП/НАСГ та порушення метаболізму глюкози в печінці. .
Як порушення кетогенезу може сприяти ураженню печінки та зміненому гомеостазу глюкози? Перше міркування полягає в тому, чи виною є дефіцит кетогенного потоку, чи самі кетони. Нещодавня доповідь свідчить про те, що кетонові тіла можуть пом’якшити пошкодження печінки, викликане окислювальним стресом, у відповідь на n-3 поліненасичені жирні кислоти (Pawlak et al., 2015). Нагадаємо, що через відсутність експресії SCOT в гепатоцитах кетонові тіла не окислюються, але вони можуть сприяти ліпогенезу та виконувати різноманітні сигнальні ролі незалежно від їх окислення (також див. Неокислювальні метаболічні долі кетонових тіл і ?OHB як сигнальний посередник). Також можливо, що кетонові тіла, отримані з гепатоцитів, можуть служити сигналом та/або метаболітом для сусідніх типів клітин у ацинусах печінки, включаючи зірчасті клітини та макрофаги клітин Купфера. Хоча обмежена доступна література свідчить про те, що макрофаги не здатні окислювати кетонові тіла, це було виміряно лише за допомогою класичних методів і лише в перитонеальних макрофагах (Newsholme et al., 1986; Newsholme et al., 1987), що вказує на те, що повторна оцінка доцільна з огляду на значну експресію SCOT в макрофагах, отриманих з кісткового мозку (Youm et al., 2015).
Кетогенний потік гепатоцитів також може бути цитопротекторним. Хоча цілющі механізми можуть не залежати від кетогенезу як такого, кетогенні дієти з низьким вмістом вуглеводів пов’язують із поліпшенням НАЖХП (Browning et al., 2011; Foster et al., 2010; Kani et al., 2014; Schugar and Crawford, 2012). . Наші спостереження показують, що кетогенез гепатоцитів може регулювати потік циклу TCA, анаплеротичний потік, глюконеогенез, отриманий з фосфоенолпірувату (Cotter et al., 2014), і навіть обмін глікогену. Кетогенне порушення спрямовує ацетил-КоА на збільшення потоку ТЦА, що в печінці пов’язують із збільшенням ушкодження, опосередкованого АФК (Satapati et al., 2015; Satapati et al., 2012); примушує переведення вуглецю в де ново синтезовані види ліпідів, які можуть виявитися цитотоксичними; і запобігає повторне окислення NADH до NAD+ (Cotter et al., 2014) (рис. 4). У сукупності необхідні майбутні експерименти, щоб розглянути механізми, завдяки яким відносна кетогенна недостатність може стати дезадаптивною, сприяти гіперглікемії, спровокувати стеатогепатит і чи діють ці механізми при НАЖХП/НАСГ людини. Епідеміологічні дані свідчать про порушення кетогенезу під час прогресування стеатогепатиту (Embade et al., 2016; Marinou et al., 2011; M�nnist� et al., 2015; Pramfalk et al., 2015; Safaei et al.), 2016 лікування, яке посилює кетогенез печінки, може виявитися корисним (Degirolamo et al., 2016; Honda et al., 2016).
Кетонові тіла та серцева недостатність (СН)
З швидкістю обміну речовин, що перевищує 400 ккал/кг/добу, і оборотом 6 кг АТФ/добу, серце є органом з найбільшою витратою енергії та окислювальною потребою (Ashrafian et al., 35; Wang et al., 2007б). Переважна більшість обороту енергії міокарда знаходиться в мітохондріях, і 2010% цього запасу надходить від ФАО. Серце є всеїдним і гнучким за нормальних умов, але серце, що патологічно ремоделює (наприклад, внаслідок гіпертонії або інфаркту міокарда), і діабетичне серце стають метаболічно негнучкими (Balasse and Fery, 70; BING, 1989; Fukao et al., 1954). ; Lopaschuk et al., 2004; Taegtmeyer et al., 2010; Taegtmeyer et al., 1980; Young et al., 2002). Справді, генетично запрограмовані аномалії метаболізму серцевого палива на моделях мишей провокують кардіоміопатію (Carley et al., 2002; Neubauer, 2014). У фізіологічних умовах нормальне серце окислює кетонові тіла пропорційно їх доставці за рахунок окислення жирних кислот і глюкози, а міокард є найбільшим споживачем кетонового тіла на одиницю маси (BING, 2007; Crawford et al., 1954; GARLAND et al. ., 2009; Hasselbaink et al., 1962; Jeffrey et al., 2003; Pelletier et al., 1995; Tardif et al., 2007; Yan et al., 2001). У порівнянні з окисленням жирних кислот, кетонові тіла більш енергетично ефективні, дають більше енергії для синтезу АТФ на молекулу кисню, що вкладається (відношення P/O) (Kashiwaya et al., 2009; Sato et al., 2010; Veech, 1995) . Окислення кетонових тіл також дає потенційно вищу енергію, ніж ФАО, підтримуючи убіхінон окисленим, що збільшує окисно-відновний діапазон у ланцюзі транспортування електронів і робить більше енергії доступним для синтезу АТФ (Sato et al., 2004; Veech, 1995). Окислення кетонових тіл також може знизити продукцію АФК і, таким чином, окислювальний стрес (Veech, 2004).
Попередні інтервенційні та обсерваційні дослідження вказують на потенційну оздоровчу роль кетонових тіл у серці. У контексті експериментального ураження ішемії/реперфузії кетонові тіла надавали потенційний кардіопротекторний ефект (Al-Zaid et al., 2007; Wang et al., 2008), можливо, через збільшення кількості мітохондрій у серці або посилення ключового окисного фосфорилювання. медіатори (Snorek et al., 2012; Zou et al., 2002). Недавні дослідження показують, що використання кетонових тіл збільшується в серцях мишей (Aubert et al., 2016) і людей (Bedi et al., 2016), що підтверджує попередні спостереження за людьми (BING, 1954; Fukao et al., 2000); Janardhan et al., 2011; Longo et al., 2004; Rudolph and Schinz, 1973; Tildon and Cornblath, 1972). Концентрації циркулюючих кетонових тіл збільшуються у пацієнтів із серцевою недостатністю, прямо пропорційно тиску наповнення, спостереження, механізм і значення яких залишаються невідомими (Kupari et al., 1995; Lommi et al., 1996; Lommi et al., 1997; Neely et al. ., 1972), але миші з селективним дефіцитом SCOT в кардіоміоцитах демонструють прискорене патологічне ремоделювання шлуночків і сигнатури АФК у відповідь на хірургічне спричинене перевантаженням тиском (Schugar et al., 2014).
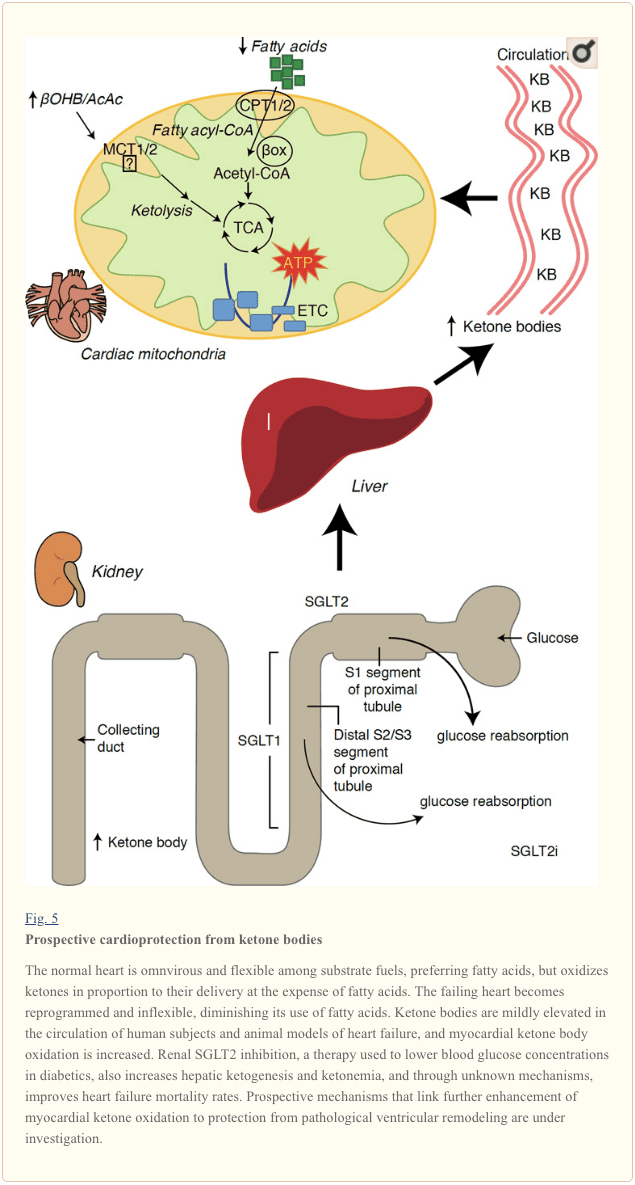
Останні інтригуючі спостереження в лікуванні діабету виявили потенційний зв’язок між метаболізмом кетонів у міокарді та патологічним ремоделюванням шлуночків (рис. 5). Інгібування ниркового проксимального канальця котранспортера натрію/глюкози 2 (SGLT2i) збільшує концентрацію циркулюючих кетонових тіл у людей (Ferrannini et al., 2016a; Inagaki et al., 2015) і мишей (Suzuki et al., 2014). кетогенез печінки (Ferrannini et al., 2014; Ferrannini et al., 2016a; Katz and Leiter, 2015; Mudaliar et al., 2015). Вражаюче, що принаймні один із цих препаратів зменшив кількість госпіталізації при СН (наприклад, як виявлено в дослідженні EMPA-REG OUTOME) та покращив серцево-судинну смертність (Fitchett et al., 2016; Sonesson et al., 2016; Wu et al., 2016a Зінман та ін., 2015). Незважаючи на те, що рушійні механізми, що стоять за сприятливими результатами HF для пов’язаного SGLT2i, залишаються предметом активних обговорень, перевага виживання, ймовірно, багатофакторна, в перспективі включає кетоз, але також благотворний вплив на вагу, кров’яний тиск, рівень глюкози та сечової кислоти, жорсткість артерій, симпатичну нервову систему, осмотичні діурез/зменшення об’єму плазми та підвищення гематокриту (Raz and Cahn, 2016; Vallon and Thomson, 2016). Взято разом, думка про те, що терапевтично наростаюча кетонемія у пацієнтів із СН або у пацієнтів із високим ризиком розвитку СН, залишається спірною, але активно досліджується в доклінічних та клінічних дослідженнях (Ferrannini et al., 2016b; Kolwicz et al., 2016; Лопащук та Верма, 2016; Мудаляр та ін., 2016; Тегтмайер, 2016).
Кетонові тіла в біології раку
Зв'язки між кетоновими тілами і раком швидко з'являються, але дослідження як на тваринах, так і на людях дали різні висновки. Оскільки кетоновий метаболізм динамічний і реагує на стан поживних речовин, є привабливим шукати біологічні зв’язки з раком через потенціал для точних методів харчування. Ракові клітини зазнають метаболічного перепрограмування для підтримки швидкої проліферації та росту клітин (DeNicola and Cantley, 2015; Pavlova and Thompson, 2016). Класичний ефект Варбурга в метаболізмі ракових клітин виникає через домінуючу роль гліколізу та молочнокислого бродіння для передачі енергії та компенсації меншої залежності від окисного фосфорилювання та обмеженого мітохондріального дихання (De Feyter et al., 2016; Grabacka et al., 2016; Kang et al., 2015; Poff et al., 2014; Shukla et al., 2014). Вуглець глюкози насамперед спрямовується через гліколіз, пентозофосфатний шлях і ліпогенез, які разом забезпечують проміжні продукти, необхідні для розширення біомаси пухлини (Grabacka et al., 2016; Shukla et al., 2014; Yoshii et al., 2015). Адаптація ракових клітин до нестачі глюкози відбувається через здатність використовувати альтернативні джерела палива, включаючи ацетат, глутамін і аспартат (Jaworski et al., 2016; Sullivan et al., 2015). Наприклад, обмежений доступ до пірувату виявляє здатність ракових клітин перетворювати глутамін в ацетил-КоА шляхом карбоксилування, підтримуючи як енергетичні, так і анаболічні потреби (Yang et al., 2014). Цікавою адаптацією ракових клітин є використання ацетату як палива (Comerford et al., 2014; Jaworski et al., 2016; Mashimo et al., 2014; Wright and Simone, 2016; Yoshii et al., 2015). Ацетат також є субстратом для ліпогенезу, який має вирішальне значення для проліферації пухлинних клітин, і збільшення цього ліпогенного каналу пов'язане з коротшим виживанням пацієнтів і більшим навантаженням на пухлину (Comerford et al., 2014; Mashimo et al., 2014; Yoshii et al. ., 2015).
Неракові клітини легко переміщають джерело енергії з глюкози на кетонові тіла під час депривації глюкози. Ця пластичність може бути більш варіабельною серед типів ракових клітин, але імплантовані пухлини мозку in vivo окислюються [2,4-13C2]-?OHB до того ж ступеня, що й навколишня тканина мозку (De Feyter et al., 2016). Моделі «зворотного ефекту Варбурга» або «метаболізму двох компартментів пухлини» припускають, що ракові клітини індукують вироблення ?OHB у сусідніх фібробластах, забезпечуючи енергетичні потреби пухлинної клітини (Bonuccelli et al., 2010; Martinez-Outschoorn et al., 2012). . У печінці зсув гепатоцитів від кетогенезу до окислення кетонів у клітинах гепатоцелюлярної карциноми (гепатоми) узгоджується з активацією активності BDH1 та SCOT, що спостерігається у двох клітинних лініях гепатоми (Zhang et al., 1989). Дійсно, клітини гепатоми експресують OXCT1 і BDH1 і окислюють кетони, але тільки при голодуванні сироватки (Huang et al., 2016). В якості альтернативи також був запропонований кетогенез пухлинних клітин. Динамічні зрушення в експресії кетогенних генів проявляються під час ракової трансформації епітелію товстої кишки, типу клітин, який зазвичай експресує HMGCS2, і в нещодавній доповіді припускається, що HMGCS2 може бути прогностичним маркером поганого прогнозу при колоректальних і плоскоклітинних карциномах (Camarero et al. 2006; Чен та ін., 2016). Чи потрібна ця асоціація кетогенез, чи підтримка функції HMGCS2, ще потрібно визначити. І навпаки, очевидна продукція ?OHB клітинами меланоми та гліобластоми, стимульована PPAR? агоніст фенофібрату, був пов’язаний із зупинкою росту (Grabacka et al., 2016). Потрібні подальші дослідження, щоб охарактеризувати роль експресії HMGCS2/SCOT, кетогенезу та окислення кетонів у ракових клітинах.
За межами паливного метаболізму кетони нещодавно були залучені в біологію ракових клітин за допомогою сигнального механізму. Аналіз меланоми BRAF-V600E+ вказав на OCT1-залежну індукцію HMGCL у онкогенний BRAF-залежний спосіб (Kang et al., 2015). Збільшення HMGCL корелювало з більш високою концентрацією AcAc в клітинах, що, в свою чергу, посилювало взаємодію BRAFV600E-MEK1, посилюючи передачу сигналів MEK-ERK у петлі прямої подачі, яка стимулює проліферацію та ріст пухлинних клітин. Ці спостереження піднімають інтригуюче питання про перспективний позапечінковий кетогенез, який потім підтримує сигнальний механізм (також див. ?OHB як сигнальний медіатор і Суперечки в позапечінковому кетогенезі). Також важливо враховувати незалежні ефекти AcAc, d-?OHB та l-?OHB на метаболізм раку, і при розгляді HMGCL катаболізм лейцину також може бути порушений.
Ефекти кетогенної дієти (також див. Терапевтичне використання кетогенної дієти та екзогенних кетонових тіл) на моделях ракових тварин різноманітні (De Feyter et al., 2016; Klement et al., 2016; Meidenbauer et al., 2015; Poff et al. ., 2014; Сейфрід та ін., 2011; Шукла та ін., 2014). Хоча епідеміологічні асоціації між ожирінням, раком і кетогенними дієтами обговорюються (Liskiewicz et al., 2016; Wright and Simone, 2016), мета-аналіз із використанням кетогенної дієти на тваринних моделях і в дослідженнях на людях припустив благотворний вплив на виживання, з переваги, проспективно пов’язані з величиною кетозу, часом початку дієти та локалізацією пухлини (Klement et al., 2016; Woolf et al., 2016). Лікування ракових клітин підшлункової залози кетоновими тілами (d-?OHB або AcAc) пригнічує ріст, проліферацію та гліколіз, а кетогенна дієта (81% ккал жирів, 18% білків, 1% вуглеводів) зменшує in vivo масу пухлини, глікемію та збільшення м’язової маси та маси тіла у тварин з імплантованим раком (Shukla et al., 2014). Подібні результати спостерігалися з використанням моделі клітин метастатичної гліобластоми у мишей, які отримували кетонові добавки в раціоні (Poff et al., 2014). І навпаки, кетогенна дієта (91% ккал жиру, 9% білка) підвищувала концентрацію ?OHB в крові та зменшувала глікемію, але не впливала ні на обсяг пухлини, ні на тривалість виживання у щурів з гліомою (De Feyter et al., 2016). Індекс глюкози кетонів був запропонований як клінічний індикатор, який покращує метаболічний контроль при лікуванні раку мозку, спричиненому кетогенною дієтою, у людей та мишей (Meidenbauer et al., 2015). Взявши разом, роль метаболізму кетонових тіл і кетонових тіл у біології раку є надзвичайними, оскільки кожен із них пропонує терапевтичні варіанти, але фундаментальні аспекти залишаються з’ясованими, з чітким впливом, що випливає з матриці змінних, включаючи (i) відмінності між екзогенним кетоном. тіла проти кетогенної дієти, (ii) тип ракової клітини, геномний поліморфізм, ступінь і стадія; і (iii) час і тривалість впливу кетотичного стану.

Кетогенез створюється кетоновими тілами шляхом розщеплення жирних кислот і кетогенних амінокислот. Цей біохімічний процес забезпечує енергією різні органи, зокрема мозок, за умов голодування як відповідь на відсутність глюкози в крові. Кетонові тіла в основному виробляються в мітохондріях клітин печінки. Хоча інші клітини здатні здійснювати кетогенез, вони не настільки ефективні в цьому, як клітини печінки. Оскільки кетогенез відбувається в мітохондріях, його процеси регулюються незалежно. Д-р Алекс Хіменес, округ Колумбія, CCST Insight
Терапевтичне застосування кетогенної дієти та екзогенних кетонових тіл
Застосування кетогенної дієти та кетонових тіл як терапевтичних засобів також виникло в неракових контекстах, включаючи ожиріння та НАЖХП/НАСГ (Browning et al., 2011; Foster et al., 2010; Schugar and Crawford, 2012); серцева недостатність (Huynh, 2016; Kolwicz et al., 2016; Taegtmeyer, 2016); неврологічні та нейродегенеративні захворювання (Martin et al., 2016; McNally and Hartman, 2012; Rho, 2015; Rogawski et al., 2016; Yang and Cheng, 2010; Yao et al., 2011); вроджені порушення метаболізму (Scholl-B�rgi et al, 2015); і виконання вправ (Cox et al., 2016). Ефективність кетогенної дієти була особливо високо оцінена в терапії епілептичних припадків, особливо у пацієнтів, стійких до ліків. Більшість досліджень оцінювали кетогенну дієту у педіатричних пацієнтів і виявляли зниження частоти нападів приблизно на 50% через 3 місяці з покращенням ефективності при окремих синдромах (Wu et al., 2016b). Досвід є більш обмеженим у дорослих епілепсії, але подібне зниження є очевидним, з кращою відповіддю у пацієнтів із симптоматичною генералізованою епілепсією (Nei et al., 2014). Основні протисудомні механізми залишаються неясними, хоча постульовані гіпотези включають зниження утилізації/гліколізу глюкози, перепрограмований транспорт глутамату, непрямий вплив на АТФ-чутливі калієві канали або рецептор аденозину A1, зміну експресії ізоформи натрієвих каналів або вплив на циркулюючий гормон (гормони, що циркулюють в крові). Lambrechts et al., 2016; Lin et al., 2017; Lutas and Yellen, 2013). Залишається незрозумілим, чи протисудомний ефект пов’язаний насамперед із кетоновими тілами, чи через каскадні метаболічні наслідки дієт з низьким вмістом вуглеводів. Тим не менш, кетонові ефіри (див. нижче), здається, підвищують поріг судом на тваринних моделях спровокованих судом (Ciarlone et al., 2016; D'Agostino et al., 2013; Viggiano et al., 2015).
Дієти з низьким вмістом вуглеводів у стилі Аткінса і кетогенні дієти часто вважаються неприємними і можуть спричинити запор, гіперурикемію, гіпокальціємію, гіпомагніємію, призвести до нефролітіазу, кетоацидозу, викликати гіперглікемію та підвищити концентрацію циркулюючого холестерину та вільної жирної кислоти 2001, Kossoff and Hartman, 2012; Kwiterovich et al., 2003; Suzuki et al., 2002). З цих причин довготривала прихильність створює проблеми. Дослідження на гризунах зазвичай використовують характерний розподіл макроелементів (94% ккал жиру, 1% ккал вуглеводів, 5% білка, Bio-Serv F3666), що провокує сильний кетоз. Однак збільшення вмісту білка навіть до 10% ккал істотно зменшує кетоз, а обмеження білка на 5% надає змішані метаболічні та фізіологічні ефекти. Цей дієтичний склад також містить холін, що є ще однією змінною, яка впливає на схильність до пошкоджень печінки і навіть на кетогенез (Garbow et al., 2011; Jornayvaz et al., 2010; Kennedy et al., 2007; Pissios et al., 2013; Schugar та ін., 2013). Вплив тривалого споживання кетогенної дієти на мишах залишається не повністю визначеним, але нещодавні дослідження на мишах показали нормальне виживання та відсутність маркерів ураження печінки у мишей на кетогенних дієтах протягом їхнього життя, хоча метаболізм амінокислот, витрата енергії та передача сигналів інсуліну. були помітно перепрограмовані (Douris et al., 2015).
Механізми, що підвищують кетоз за допомогою механізмів, альтернативних кетогенним дієтам, включають використання попередників кетонових тіл, які вживаються всередину. Введення екзогенних кетонових тіл може створити унікальний фізіологічний стан, який не зустрічається в нормальній фізіології, оскільки концентрації циркулюючої глюкози та інсуліну є відносно нормальними, тоді як клітини можуть знижувати поглинання та використання глюкози. Самі кетонові тіла мають короткий період напіврозпаду, і прийом або вливання солі натрію ?OHB для досягнення терапевтичного кетозу провокує небажане навантаження натрієм. R/S-1,3-бутандіол є нетоксичним діаспиртом, який легко окислюється в печінці з утворенням d/l-?OHB (Desrochers et al., 1992). У різних експериментальних контекстах цю дозу вводили щодня мишам або щурам протягом семи тижнів, що дає циркулюючі концентрації ?OHB до 5 мМ протягом 2 годин після введення, які стабільні протягом щонайменше додаткових 3 годин (D' Агостіно та ін., 2013). Часткове пригнічення споживання їжі спостерігалося у гризунів, які отримували R/S-1,3-бутандіол (Carpenter and Grossman, 1983). Крім того, три хімічно різні ефіри кетонів (KEs), (i) моноефір R-1,3-бутандиолу та d-?OHB (R-3-гідроксибутил R-?OHB); (ii) гліцерил-трис-?OHB; і (iii) диефір ацетоацетату R,S-1,3-бутандиолу також були детально вивчені (Brunengraber, 1997; Clarke et al., 2012a; Clarke et al., 2012b; Desrochers et al., 1995a; Desrochers et al. ., 1995b; Kashiwaya et al., 2010). Невід'ємною перевагою першого є те, що після гідролізу естерази в кишечнику або печінці на моль KE утворюється 2 моль фізіологічного d-?OHB. Безпека, фармакокінетика та переносимість були найбільш детально вивчені у людей, які споживали R-3-гідроксибутил R-?OHB в дозах до 714 мг/кг, що давало циркулюючі концентрації d-?OHB до 6 мМ (Clarke et al., 2012a; Cox et al., 2016; Kemper et al., 2015; Shivva et al., 2016). У гризунів цей KE зменшує споживання калорій і загальний холестерин плазми, стимулює буру жирову тканину та покращує резистентність до інсуліну (Kashiwaya et al., 2010; Kemper et al., 2015; Veech, 2013). Останні результати свідчать про те, що під час фізичних навантажень у тренованих спортсменів прийом R-3-гідроксибутил R-?OHB в скелетних м’язах знижував гліколіз скелетних м’язів і концентрацію лактату в плазмі, посилював внутрішньом’язове окислення триацилгліцерину та зберігав вміст м’язового глікогену, навіть коли одночасно стимулювався секреція інсуліну (стимуляція секреції інсуліну). Кокс та ін., 2016). Потрібна подальша розробка цих інтригуючих результатів, оскільки покращення продуктивності вправ на витривалість переважно було зумовлено стійкою реакцією на КЕ у 2/8 суб’єктів. Тим не менш, ці результати підтверджують класичні дослідження, які вказують на перевагу окислення кетонів перед іншими субстратами (GARLAND et al., 1962; Hasselbaink et al., 2003; Stanley et al., 2003; Valente-Silva et al., 2015), в тому числі під час вправ, і що треновані спортсмени можуть бути більш підготовленими до використання кетонів (Johnson et al., 1969a; Johnson and Walton, 1972; Winder et al., 1974; Winder et al., 1975). Нарешті, механізми, які можуть підтримувати покращення продуктивності вправи після рівного споживання калорій (по-різному розподіленого між макроелементами) та рівного споживання кисню, ще потрібно визначити.
Майбутня перспектива
Після того, як значною мірою стигматизували як шлях переповнення, здатний накопичувати токсичні викиди від спалювання жиру в станах з обмеженим вмістом вуглеводів (парадигма «кетотоксичності»), останні спостереження підтверджують ідею, що метаболізм кетонових тіл виконує оздоровчу роль навіть у станах, насичених вуглеводами, відкриваючи «кетогорметик». � гіпотеза. Хоча легкі харчові та фармакологічні підходи до маніпулювання метаболізмом кетонів роблять його привабливою терапевтичною метою, агресивно поставлені, але розважливі експерименти залишаються як у базових, так і в трансляційних дослідницьких лабораторіях. Незадоволені потреби виникли у сферах визначення ролі метаболізму кетонів при серцевій недостатності, ожирінні, НАЖХП/НАСГ, діабеті 2 типу та раку. Обсяг і вплив «неканонічних» сигнальних ролей кетонових тіл, включаючи регуляцію PTM, які, ймовірно, повертаються і переходять у метаболічні та сигнальні шляхи, потребують більш глибокого дослідження. Нарешті, позапечінковий кетогенез може відкрити інтригуючі паракринні та аутокринні сигнальні механізми та можливості впливати на сумісний метаболізм у нервовій системі та пухлинах для досягнення терапевтичних цілей.
Подяки
Ncbi.nlm.nih.gov/pmc/articles/PMC5313038/
Виноски
На закінчення, кетонові тіла виробляються печінкою для того, щоб використовуватися як джерело енергії, коли в організмі людини недостатньо глюкози. Кетогенез виникає, коли в крові низький рівень глюкози, особливо після того, як інші клітинні запаси вуглеводів вичерпані. Метою статті вище було обговорити багатовимірну роль кетонових тіл у паливному метаболізмі, передачі сигналів та терапевтиці. Обсяг нашої інформації обмежено хіропрактикою та проблемами здоров’я хребта. Щоб обговорити тему, зверніться до доктора Хіменеса або зв’яжіться з нами за адресою�915-850-0900.
Куратор доктор Алекс Хіменес
Посилання на: �Ncbi.nlm.nih.gov/pmc/articles/PMC5313038/

Додаткова тема для обговорення: «Гострий біль у спині».
Біль у спині� є однією з найпоширеніших причин інвалідності та пропущених робочих днів у всьому світі. Біль у спині є другою за поширеністю причиною відвідувань лікаря, переважаючи лише інфекції верхніх дихальних шляхів. Приблизно 80 відсотків населення відчувають біль у спині хоча б раз у житті. Хребет – це складна структура, що складається з кісток, суглобів, зв’язок і м’язів, серед інших м’яких тканин. Травми та/або загострені стани, такі як �грижі диски, може зрештою призвести до симптомів болю в спині. Спортивні травми або травми в автомобільній катастрофі часто є найчастішою причиною болю в спині, однак іноді найпростіші рухи можуть мати хворобливі наслідки. На щастя, альтернативні варіанти лікування, такі як хіропрактика, можуть допомогти полегшити біль у спині за допомогою корекції хребта та ручних маніпуляцій, що в кінцевому підсумку покращує полегшення болю. �

ЕКСТРА ДОДАТКО | ВАЖЛИВА ТЕМА: Рекомендований хіропрактик в Ель-Пасо, штат Техас
***
Інформація в цьому документі на "Багатовимірні ролі кетонових тіл" не призначений для заміни особистих стосунків із кваліфікованим медичним працівником або ліцензованим лікарем і не є медичною консультацією. Ми заохочуємо вас приймати рішення щодо охорони здоров’я на основі ваших досліджень і партнерства з кваліфікованим медичним працівником.
Інформація в блозі та обговорення обсягу
Наша інформаційна сфера обмежується хіропрактикою, опорно-руховим апаратом, фізичними препаратами, оздоровленням, що сприяє етіологічному вісцеросоматичні порушення у клінічних презентаціях, клінічній динаміці асоційованого соматовісцерального рефлексу, комплексах підвивиху, чутливих питаннях здоров’я та/або статей, темах та дискусіях з функціональної медицини.
Надаємо та презентуємо клінічне співробітництво з фахівцями різних галузей. Кожен фахівець керується своєю професійною сферою практики та юрисдикцією ліцензування. Ми використовуємо протоколи функціонального здоров’я та оздоровлення для лікування та підтримки догляду за травмами або розладами опорно-рухового апарату.
Наші відео, дописи, теми, предмети та висновки охоплюють клінічні питання, проблеми та теми, які стосуються та прямо чи опосередковано підтримують нашу клінічну практику.*
Наш офіс обґрунтовано намагався надати підтверджувальні цитати та визначив відповідне дослідження або дослідження, що підтверджують наші публікації. За запитом ми надаємо копії допоміжних наукових досліджень, доступні регуляторним комісіям та громадськості.
Ми розуміємо, що ми розглядаємо питання, які потребують додаткового пояснення того, як це може допомогти в певному плані догляду або протоколі лікування; тому для подальшого обговорення вищезазначеної теми, будь ласка, не соромтеся запитувати Доктор Алекс Хіменес, округ Колумбія, Або зв'яжіться з нами за адресою 915-850-0900.
Ми тут, щоб допомогти вам та вашій родині.
Благословення
Д-р Алекс Хіменес Постійного струму, MSACP, RN*, CCST, IFMCP*, CIFM*, ATN*
електронна пошта: coach@elpasofunctionalmedicine.com
Ліцензія доктора хіропрактики (DC) у Техас & Нью-Мексико*
Техас, округ Колумбія, номер ліцензії TX5807, Нью-Мексико, округ Колумбія Номер ліцензії NM-DC2182
Ліцензія дипломованої медсестри (RN*) in Флорида
Ліцензія Флориди Ліцензія RN # RN9617241 (Контрольний номер 3558029)
Компактний статус: Мультидержавна ліцензія: Уповноважений на практику в Стани 40*
Доктор Алекс Хіменес, округ Колумбія, MSACP, RN* CIFM*, IFMCP*, ATN*, CCST
Моя цифрова візитна картка