зміст
рак
Дослідження показали, що миші, які не експресують NRF2, більш схильні до розвитку раку у відповідь на фізичну та хімічну стимуляцію. Однак подібні дослідження показали, що надмірна активація NRF2 або навіть інактивація KEAP1 може призвести до загострення деяких видів раку, особливо якщо ці шляхи були перервані. Надмірна активність NRF2 може виникнути через куріння, де безперервна активація NRF2 вважається причиною раку легенів у курців. Надмірна експресія Nrf2 може призвести до того, що ракові клітини не самознищуються, тоді як періодична активація NRF2 може запобігти індукції токсинів раковими клітинами. Крім того, оскільки надекспресія NRF2 збільшує антиоксидантну здатність людського організму функціонувати за межами окислювально-відновного гомеостазу, це посилює поділ клітин і створює неприродну схему метилювання ДНК та гістонів. Це в кінцевому підсумку може зробити хіміотерапію та променеву терапію менш ефективними проти раку. Тому обмеження активації NRF2 такими речовинами, як DIM, лютеолін, Zi Cao або саліноміцин, може бути ідеальним для пацієнтів з раком, хоча надмірна активація Nrf2 не повинна розглядатися як єдина причина раку. Дефіцит поживних речовин може вплинути на гени, включаючи NRF2. Це може бути одним із способів того, як недоліки сприяють утворенню пухлин.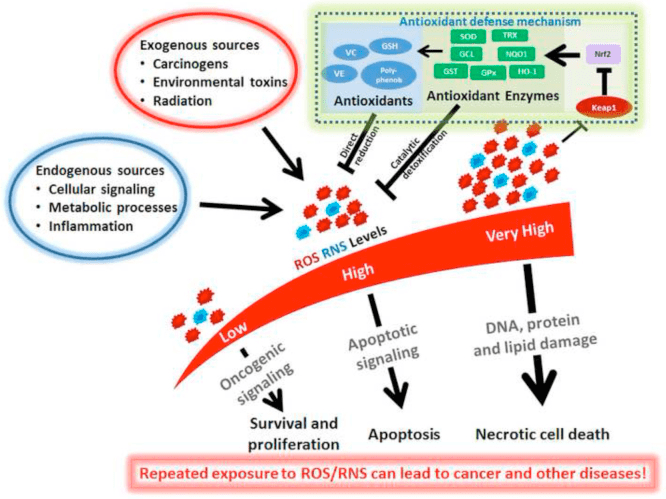
Печінка
Надактивація Nrf2 також може вплинути на функцію окремих органів в організмі людини. Надмірна експресія NRF2 може в кінцевому підсумку блокувати вироблення інсуліноподібного фактора росту 1, або IGF-1, у печінці, який є важливим для регенерації печінки.Серце
У той час як гостра надекспресія Nrf2 може мати свої переваги, постійна надекспресія NRF2 може викликати довгострокові шкідливі ефекти на серце, такі як кардіоміопатія. Експресія NRF2 може бути збільшена за рахунок високого рівня холестерину або активації HO-1. Вважається, що це є причиною того, що хронічний підвищений рівень холестерину може викликати проблеми зі здоров'ям серцево-судинної системи.Вітіліго
Також було продемонстровано, що надмірна експресія NRF2 пригнічує здатність до репігментації при вітіліго, оскільки вона може перешкоджати дії тирозинази або TYR, яка є важливою для репігментації через меланіногенез. Дослідження показали, що цей процес може бути однією з основних причин того, чому люди з вітіліго, здається, не активують Nrf2 так само ефективно, як люди без вітіліго.Чому NRF2 може не функціонувати належним чином
Хормесіс
NRF2 має бути активований горметично, щоб мати можливість скористатися його перевагами. Іншими словами, Nrf2 не повинен запускатися щохвилини або щодня, тому було б чудовою ідеєю робити перерви, наприклад, 5 днів на 5 вихідних або через день. NRF2 також повинен досягти певного порогу, щоб запустити його гормональну реакцію, де невеликого стресора може бути недостатньо, щоб його запустити.DJ-1 Окислення
Білкова дегліказа DJ-1, або просто DJ-1, також званий білком хвороби Паркінсона, або PARK7, є головним регулятором і детектором окислювально-відновного статусу в організмі людини. DJ-1 має важливе значення для регулювання того, як довго NRF2 може виконувати свою функцію та виробляти антиоксидантну відповідь. У разі надмірного окислення DJ-1 клітини зроблять білок DJ-1 менш доступним. Цей процес спонукає активацію NRF2 занадто швидко закінчуватися, оскільки DJ-1 має першорядне значення для підтримки збалансованих рівнів NRF2 і запобігання їх розпаду в клітині. У випадку, якщо білок DJ-1 не існує або переокислений, експресія NRF2, ймовірно, буде мінімальною, навіть за допомогою DIM або альтернативних активаторів NRF2. Експресія DJ-1 необхідна для відновлення порушеної дії NRF2.Хронічні захворювання
Якщо у вас є хронічні захворювання, включаючи CIRS, хронічні інфекції/дисбактеріоз/SIBO, або накопичення важких металів, таких як ртуть та/або з кореневих каналів, це може перешкоджати системам NRF2 та фазі детоксикації. Замість того, щоб окислювальний стрес перетворював NRF2 на антиоксидант, NRF2 не спрацьовує, і окислювальний стрес може залишатися в клітині і спричиняти пошкодження, тобто антиоксидантної реакції немає. Це важлива причина, чому багато людей з CIRS мають кілька чутливих і схильні до численних факторів. Деякі люди вважають, що вони можуть мати реакцію herx, однак ця реакція може лише пошкоджувати клітини далі. Лікування хронічних захворювань, однак, дозволить печінці викидати токсини в жовч, поступово розвиваючи горметичну відповідь активації NRF2. Якщо жовч залишається токсичною і не виводиться з організму людини, вона відновить окислювальний стрес NRF2 і спричинить погіршення самопочуття після того, як вона повторно всмоктується з шлунково-кишкового тракту або шлунково-кишкового тракту. Наприклад, охратоксин А може блокувати NRF2. Крім лікування проблеми, інгібітори гістондеацетилази можуть блокувати окислювальну реакцію ряду факторів, які викликають активацію NRF2, але вони також можуть перешкоджати нормальному запуску NRF2, що в кінцевому підсумку може не виконувати своєї мети.Порушення регуляції риб’ячого жиру
Холінергічні речовини – це речовини, які підвищують ацетилхолін, або ACh, і холін в мозку через збільшення ACh, особливо при пригніченні розпаду ACh. Пацієнти з CIRS часто мають проблеми з порушенням регуляції рівня ацетилхоліну в організмі людини, особливо в мозку. Риб’ячий жир запускає NRF2, активуючи його захисний антиоксидантний механізм у клітинах. Люди з хронічними захворюваннями можуть мати проблеми з когнітивним стресом і ексайтотоксичністю ацетилхоліну через накопичення фосфаторганічних речовин, що може призвести до того, що риб’ячий жир викликає запалення в організмі людини. Дефіцит холіну додатково викликає активацію NRF2. Включення холіну у ваш раціон (поліфенолів, яєць тощо) може допомогти посилити ефекти холінергічної дисрегуляції.Що зменшує NRF2?
Зменшення надмірної експресії NRF2 найкраще для людей з раком, хоча це може бути корисно для багатьох інших проблем зі здоров’ям.Дієта, харчові добавки та звичайні ліки:
- Апігенін (вищі дози)
- Бруцея яванська
- Каштани
- EGCG (високі дози збільшують NRF2)
- Пажитник (тригонелін)
- Hiba (хінокітіол/?-туяпліцин)
- Дієта з високим вмістом солі
- Лютеолін (селера, зелений перець, петрушка, лист перілли та ромашковий чай – більш високі дози можуть збільшити NRF2 – 40 мг/кг лютеоліну тричі на тиждень)
- Метформін (хронічний прийом)
- N-ацетил-L-цистеїн (NAC, блокуючи окислювальну відповідь, особливо у високих дозах)
- Цедра апельсина (має поліметоксильовані флавоноїди)
- Кверцетин (вищі дози можуть збільшити NRF2 – 50 мг/кг/день кверцетину)
- Саліноміцин (лікарський засіб)
- Ретинол (повністю транс-ретиноева кислота)
- Вітамін С у поєднанні з кверцетином
- Цзи Цао (Пурпурний Громвел має Шиконін/Алканін)
Шляхи та інше:
- Бах1
- BET
- Біоплівки
- Брусатол
- Камптотецин
- DNMT
- DPP-23
- EZH2
- Передача сигналів глюкокортикоїдних рецепторів (дексаметазон і бетаметазон також)
- ГСК-3? (регуляторний зворотній зв'язок)
- Активація HDAC?
- Галофугінон
- Гомоцистеїн (ALCAR може змінити цей гомоцистеїн, що викликає низькі рівні NRF2)
- IL-24
- Keep1
- MDA-7
- NF?B
- Охратоксин А (види Aspergillus і pencicllium)
- Білок промієлоцитарної лейкемії
- p38
- p53
- p97
- Альфа-рецептор ретиноєвої кислоти
- селеніт
- SYVN1 (Hrd1)
- Інгібування STAT3 (наприклад, криптотаншинон)
- Тестостерон (і тестостерону пропіонат, хоча TP інтраназально може збільшити NRF2)
- Trecator (етіонамід)
- Trx1 (через зменшення Cys151 в Keap1 або Cys506 в області NLS Nrf2)
- Тролокс
- Вориностат
- Дефіцит цинку (погіршує роботу мозку)
Nrf2 Механізм дії
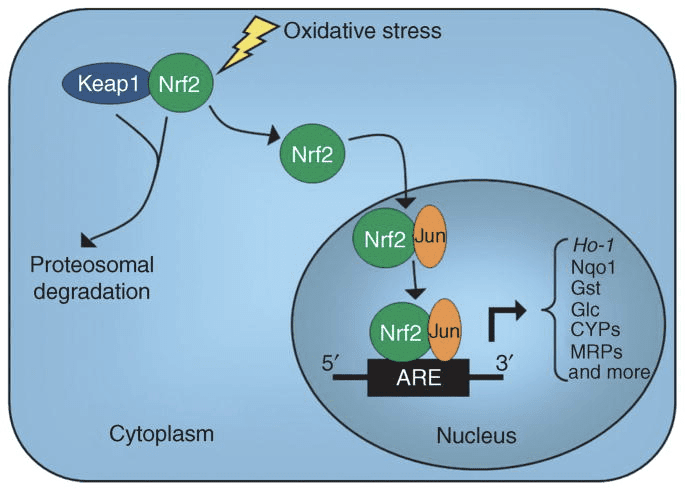
- Збільшує AKR
- Збільшує АРЕ
- Підвищує ATF4
- Збільшує Bcl-xL
- Підвищує Bcl-2
- Підвищує BDNF
- Збільшує BRCA1
- Збільшує c-червень
- Збільшує CAT
- Підвищує цГМФ
- Підвищує CKIP-1
- Підвищує CYP450
- Збільшує Cul3
- Підвищує ГКЛ
- Збільшує GCLC
- Збільшує GCLM
- Підвищує ГКС
- Збільшує GPx
- Збільшує GR
- Підвищує GSH
- Збільшує податок на товари та послуги
- Збільшує HIF1
- Підвищує HO-1
- Підвищує HQO1
- Підвищує HSP70
- Підвищує рівень ІЛ-4
- Підвищує рівень ІЛ-5
- Підвищує рівень ІЛ-10
- Підвищує рівень ІЛ-13
- Збільшує К6
- Збільшує К16
- Збільшує К17
- Збільшує mEH
- Збільшує Mrp2-5
- Підвищує НАДФН
- Підвищує рівень 1
- Збільшує NQO1
- Підвищує PPAR-альфа
- Збільшує Prx
- Збільшує р62
- Збільшує Sesn2
- Збільшує Slco1b2
- Збільшує sMafs
- Збільшує СОД
- Збільшує Trx
- Збільшує Txn(d)
- Збільшує UGT1(A1/6)
- Підвищує VEGF
- Зменшує ADAMTS (4/5)
- Знижує альфа-SMA
- Знижує АЛТ
- Зменшує AP1
- Знижує АСТ
- Зменшує Бах1
- Знижує ЦОГ-2
- Зменшує DNMT
- Знижує FASN
- Знижує FGF
- Зменшує HDAC
- Знижує IFN-?
- Знижує IgE
- Знижує IGF-1
- Знижує рівень IL-1b
- Знижує рівень ІЛ-2
- Знижує рівень ІЛ-6
- Знижує рівень ІЛ-8
- Знижує рівень ІЛ-25
- Знижує рівень ІЛ-33
- Зменшує iNOS
- Знижує LT
- Зменшує Keap1
- Знижує MCP-1
- Знижує MIP-2
- Знижує MMP-1
- Знижує MMP-2
- Знижує MMP-3
- Знижує MMP-9
- Знижує MMP-13
- Зменшує NfkB
- Зменшує NO
- Зменшує SIRT1
- Знижує TGF-b1
- Знижує TNF-альфа
- Знижує Tyr
- Зменшує VCAM-1
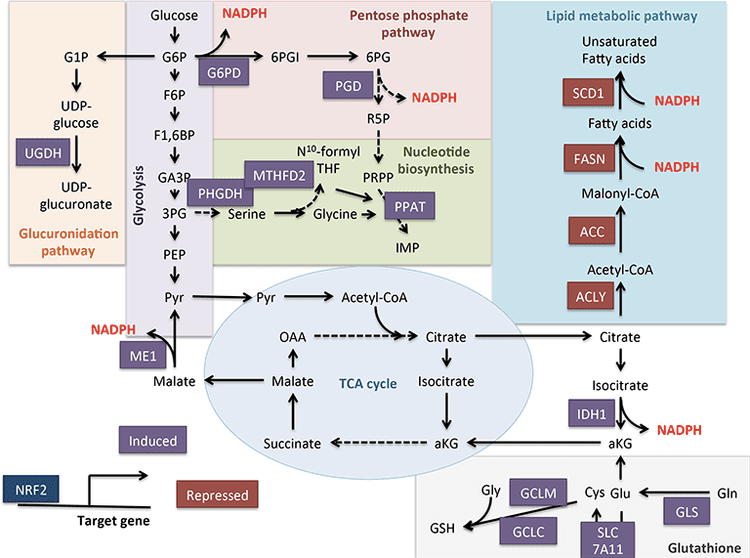
- Закодований з гена NFE2L2, NRF2 або фактор 2, пов’язаний з ядерним еритроїдом 2, є фактором транскрипції в базовій лейциновій блискавці, або bZIP, надсімействі, яка використовує Cap'n'Collar, або структуру CNC.
- Він стимулює азотні ферменти, ферменти біотрансформації та транспортери витоку ксенобіотиків.
- Це важливий регулятор при індукції генів антиоксидантів і ферментів детоксикації фази II, які захищають клітини від пошкоджень, спричинених окислювальним стресом та електрофільними атаками.
- Під час гомеостатичних умов Nrf2 секвеструється в цитозолі шляхом тілесного приєднання N-кінцевого домену Nrf2 або Kelch-подібного ECH-асоційованого білка або Keap1, також званого INrf2 або інгібітором Nrf2, інгібуючи активацію Nrf2.
- Він також може контролюватися за допомогою селенопротеїну тіоредоксин редуктази 1 ссавців або TrxR1, який функціонує як негативний регулятор.
- Після вразливості до електрофільних стресорів Nrf2 відокремлюється від Keap1, переміщаючись у ядро, де потім гетеродимеризується за допомогою ряду білків-регуляторів транскрипції.
- Часті взаємодії включають такі взаємодії органів транскрипції Jun і Fos, які можуть бути членами сімейства білків-активаторів факторів транскрипції.
- Після димеризації ці комплекси зв’язуються з компонентами ARE/EpRE, які реагують на антиоксиданти/електрофіли, і активують транскрипцію, як це стосується комплексу Jun-Nrf2, або пригнічують транскрипцію, подібно до комплексу Fos-Nrf2.
- Позиціонування ARE, яке запускається або пригнічується, визначить, які гени транскрипційно контролюються цими змінними.
- Коли активується ARE:
- Активація синтезу антиоксидантів здатна детоксикувати АФК, як каталаза, супероксиддисмутаза або СОД, GSH-пероксидаза, GSH-редуктаза, GSH-трансфераза, НАДФН-хіноноксидоредуктаза або NQO1, цитохром Р450, моноокситіогеназа, система цитохрому Р70 редуктаза і HSPXNUMX.
- Активація цієї GSH-синтази забезпечує помітне зростання внутрішньоклітинного рівня GSH, що є досить захисним.
- Посилення цього синтезу та ступеня ферментів фази II, таких як UDP-глюкуронозилтрансфераза, N-ацетилтрансферази та сульфотрансферази.
- Підвищення регуляції HO-1, який є дійсно захисним рецептором з потенційним зростанням CO, що в поєднанні з NO дозволяє вазодилатацію ішемізованих клітин.
- Зменшення перевантаження залізом за рахунок підвищення рівня феритину та білірубіну як ліпофільного антиоксиданту. Обидва білки фази II разом з антиоксидантами здатні фіксувати хронічний окислювальний стрес, а також відновлювати нормальну окислювально-відновну систему.
- GSK3? під керівництвом AKT і PI3K фосфорилює Fyn, що призводить до ядерної локалізації Fyn, яка Fyn фосфорилює Nrf2Y568, що призводить до ядерного експорту та деградації Nrf2.
- NRF2 також послаблює реакцію TH1/TH17 і збагачує відповідь TH2.
- Інгібітори HDAC ініціювали сигнальний шлях Nrf2 і регулювали, що нижній Nrf2 спрямований на HO-1, NQO1 і каталітичну субодиницю глутамат-цистеїн-лігази або GCLC, стримуючи Keap1 і заохочуючи дисоціацію Keap1 від Nrf2, Nrflo і Nrf2. - Є обов'язковими.
- Nrf2 включає період напіввиведення приблизно 20 хвилин у базальних умовах.
- Зменшення IKK? пул через прив'язку Keap1 зменшує I?B? деградація і може бути невловимим механізмом, за допомогою якого було доведено, що активація Nrf2 інгібує активацію NF?B.
- Keap1 не завжди потрібно знижувати, щоб NRF2 працював, наприклад хлорофілін, чорниця, елагова кислота, астаксантин і поліфеноли чаю можуть підвищити NRF2 і KEAP1 на 400 відсотків.
- Nrf2 регулює негативно через термін стеароіл-КоА-десатурази, або SCD, і цитрат-ліази, або CL.
Генетика
KEAP1
rs1048290
- Алель C – показав значний ризик і захисний ефект проти лікарсько-резистентної епілепсії (DRE)
rs11085735 (я AC)
- пов'язаний зі швидкістю зниження функції легенів у LHS
КАРТА
rs242561
- Алель T – захисний алель для паркінсонічних розладів – мав міцніше зв’язування NRF2/sMAF і був пов’язаний з вищими рівнями мРНК MAPT у 3 різних областях мозку, включаючи кору мозочка (CRBL), скроневу кору (TCTX), внутрішньодолькову білу речовину (WHMT).
NFE2L2 (NRF2)
rs10183914 (я CT)
- Алель T – підвищення рівня білка Nrf2 і відстрочений вік початку хвороби Паркінсона на чотири роки
rs16865105 (я AC)
- Алель С – мав більший ризик хвороби Паркінсона
rs1806649 (я CT)
- Алель C – був ідентифікований і може мати значення для етіології раку молочної залози.
- пов’язані з підвищеним ризиком госпіталізації в періоди високого рівня PM10
rs1962142 (я GG)
- Алель T – асоціюється з низьким рівнем експресії NRF2 в цитоплазмі (P = 0.036) і негативною експресією сульфіредоксину (P = 0.042)
- Алель – захищений від зниження кровотоку передпліччя (FEV) (об’єм форсованого видиху за одну секунду) по відношенню до куріння сигарети (p = 0.004)
rs2001350 (я TT)
- Алель T – захищений від зниження ОФВ (об’єм форсованого видиху за одну секунду) по відношенню до куріння сигарети (р = 0.004)
rs2364722 (я AA)
- Алель – захищений від зниження ОФВ (об’єм форсованого видиху за одну секунду) по відношенню до куріння сигарети (р = 0.004)
rs2364723
- Алель С – пов’язаний зі значно зниженим ОФВ у японських курців з раком легенів
rs2706110
- Алель G – показав значний ризик і захисний ефект проти епілепсії, резистентної до ліків (DRE)
- Алелі AA – показали значно знижену експресію KEAP1
- Алелі AA – були пов’язані з підвищеним ризиком раку молочної залози (P = 0.011)
rs2886161 (я TT)
- Алель Т - пов'язана з хворобою Паркінсона
rs2886162
- Алель – був пов’язаний з низькою експресією NRF2 (P = 0.011; OR, 1.988; CI, 1.162×3.400), а генотип AA був пов’язаний з гіршою виживаністю (P = 0.032; HR, 1.687; CI, 1.047×2.748)
rs35652124 (я TT)
- Алель – пов’язаний з вищим, пов’язаним із віком на початку хвороби Паркінсона проти алеля G
- Алель С – мав збільшення білка NRF2
- Алель T – мав менше білка NRF2 і більший ризик серцевих захворювань і кров’яного тиску
rs6706649 (я CC)
- Алель C – мав нижчий білок NRF2 і підвищував ризик хвороби Паркінсона
rs6721961 (я GG)
- Алель Т – мав нижчий білок NRF2
- Алелі ТТ – зв’язок між курінням сигарет у завзятих курців і зниженням якості сперми
- Алель TT – асоціюється з підвищеним ризиком раку молочної залози [P = 0.008; АБО 4.656; довірчий інтервал (CI), 1.350×16.063] і алель T були пов’язані з низькою ступенем експресії білка NRF2 (P = 0.0003; OR, 2.420; CI, 1.491×3.926) та негативною експресією SRXN1 (P = 0.047; OR; 1.867; CI = 1.002�3.478)
- Алель T – алель також був номінально пов’язаний із 28-денною смертністю, пов’язаною з ALI, після синдрому системної запальної відповіді
- Алель T – захищений від зниження ОФВ (об’єм форсованого видиху за одну секунду) по відношенню до куріння сигарети (р = 0.004)
- Алель G – пов’язаний з підвищеним ризиком розвитку ALI після серйозної травми у європейців та афроамериканців (відношення шансів, АБО 6.44; 95% довірчий інтервал
- Алелі AA – пов’язані з астмою, спричиненою інфекцією
- Алелі AA – демонстрували значно знижену експресію гена NRF2 і, як наслідок, підвищений ризик раку легенів, особливо тих, хто коли-небудь курив
- Алелі AA – мали значно вищий ризик розвитку ЦД 2 типу (OR 1.77; 95% ДІ 1.26, 2.49; p = 0.011) порівняно з тими, хто має генотипом CC
- Алелі AA – сильний зв’язок між відновленням ран і пізньою токсичністю радіації (пов’язаний зі значно більш високим ризиком розвитку пізніх наслідків у афроамериканців з тенденцією у європеоїдної раси)
- пов’язані з пероральною терапією естрогенами та ризиком венозної тромбоемболії у жінок у постменопаузі
rs6726395 (я AG)
- Алель – захищений від зниження ОФВ1 (об’єм форсованого видиху за одну секунду) по відношенню до куріння сигарети (р = 0.004)
- Алель – пов’язаний зі значно зниженим ОФВ1 у японських курців з раком легенів
- Алелі GG – мали вищі рівні NRF2 і знижений ризик макулярної дегенерації
- Алелі GG – мали вищу виживаність при холангіокарциномі
rs7557529 (я CT)
- Алель С - пов'язана з хворобою Паркінсона

Окислювальний стрес та інші стресори можуть викликати пошкодження клітин, що в кінцевому підсумку може призвести до різноманітних проблем зі здоров’ям. Дослідження показали, що активація Nrf2 може сприяти захисному антиоксидантному механізму людського організму, однак дослідники обговорювали, що надмірна експресія Nrf2 може мати величезні ризики для загального здоров’я та самопочуття. Різні типи раку також можуть виникати при надмірній активації Nrf2. Д-р Алекс Хіменес, округ Колумбія, CCST Insight
Сульфорафан та його вплив на рак, смертність, старіння, мозок і поведінку, хвороби серця тощо
- 00:01:14 – Рак і смертність
- 00:19:04 – Старіння
- 00:26:30 – Мозок і поведінка
- 00:38:06 – Підсумок
- 00:40:27 – Доза
- 00:00:34 – Представлення сульфорафану, головна тема відео.
- 00:01:14 – Споживання овочів хрестоцвітних і зниження смертності від усіх причин.
- 00:02:12 – Ризик раку передміхурової залози.
- 00:02:23 – Ризик раку сечового міхура.
- 00:02:34 – Ризик раку легенів у курців.
- 00:02:48 – Ризик раку молочної залози.
- 00:03:13 – Гіпотетична: що робити, якщо у вас уже рак? (інтервенційний)
- 00:03:35 – Імовірний механізм, який керує асоціативними даними раку та смертності.
- 00:04:38 – Сульфорафан і рак.
- 00:05:32 – Докази на тваринах, що показують сильний вплив екстракту паростків брокколі на розвиток пухлин сечового міхура у щурів.
- 00:06:06 – Вплив прямого прийому сульфорафану у пацієнтів з раком передміхурової залози.
- 00:07:09 – Біоакумуляція метаболітів ізотіоціаната у фактичній тканині молочної залози.
- 00:08:32 – Пригнічення стовбурових клітин раку молочної залози.
- 00:08:53 – Урок історії: ще в Стародавньому Римі стверджували, що капустяні гриби мають оздоровчі властивості.
- 00:09:16 – Здатність сульфорафану посилювати виведення канцерогену (бензолу, акролеїну).
- 00:09:51 – NRF2 як генетичний перемикач через елементи антиоксидантної реакції.
- 00:10:10 – Як активація NRF2 посилює виведення канцерогену через глутатіон-S-кон'югати.
- 00:10:34 – Брюссельська капуста підвищує глутатіон-S-трансферазу і зменшує пошкодження ДНК.
- 00:11:20 – Напій з проростків брокколі збільшує виведення бензолу на 61%.
- 00:13:31 – Гомогенат паростків брокколі підвищує антиоксидантні ферменти у верхніх дихальних шляхах.
- 00:15:45 – Споживання хрестоцвітних овочів і смертність від серцево-судинних захворювань.
- 00:16:55 – порошок паростків брокколі покращує рівень ліпідів у крові та загальний ризик серцевих захворювань у діабетиків 2 типу.
- 00:19:04 – Початок секції старіння.
- 00:19:21 – Дієта, збагачена сульфорафаном, збільшує тривалість життя жуків від 15 до 30% (за певних умов).
- 00:20:34 – Важливість слабкого запалення для довголіття.
- 00:22:05 – Овочі хрестоцвітних і порошок паростків брокколі, здається, зменшують широкий спектр запальних маркерів у людей.
- 00:23:40 – Підсумок у середині відео: розділи про рак, старіння
- 00:24:14 – Дослідження на мишах показують, що сульфорафан може покращити адаптивну імунну функцію в літньому віці.
- 00:25:18 – Сульфорафан покращив ріст волосся у мишачої моделі облисіння. Зображення на 00:26:10.
- 00:26:30 – Початок розділу «Мозок і поведінка».
- 00:27:18 – Вплив екстракту паростків брокколі на аутизм.
- 00:27:48 – Вплив глюкорафаніну на шизофренію.
- 00:28:17 – Початок обговорення депресії (правдоподібний механізм та дослідження).
- 00:31:21 – Дослідження на мишах з використанням 10 різних моделей депресії, викликаної стресом, показало, що сульфорафан так само ефективний, як і флуоксетин (прозак).
- 00:32:00 – Дослідження показує, що пряме вживання глюкорафаніну мишами так само ефективне для запобігання депресії через модель стресу соціальної поразки.
- 00:33:01 – Початок відділу нейродегенерації.
- 00:33:30 – Сульфорафан і хвороба Альцгеймера.
- 00:33:44 – Сульфорафан і хвороба Паркінсона.
- 00:33:51 – Сульфорафан і хвороба Хантінгтона.
- 00:34:13 – Сульфорафан збільшує кількість білків теплового шоку.
- 00:34:43 – Початок секції черепно-мозкової травми.
- 00:35:01 – Сульфорафан, введений відразу після ЧМТ, покращує пам’ять (дослідження на мишах).
- 00:35:55 – Сульфорафан і нейрональна пластичність.
- 00:36:32 – Сульфорафан покращує навчання на моделі діабету ІІ типу у мишей.
- 00:37:19 – Сульфорафанова і м’язова дистрофія Дюшенна.
- 00:37:44 – Інгібування міостатину в клітинах-супутниках м’язів (in vitro).
- 00:38:06 – Пізнє відео: смертність і рак, пошкодження ДНК, окислювальний стрес і запалення, виділення бензолу, серцево-судинні захворювання, діабет ІІ типу, вплив на мозок (депресія, аутизм, шизофренія, нейродегенерація), шлях NRF2.
- 00:40:27 – Думки щодо визначення дози паростків брокколі або сульфорафану.
- 00:41:01 – Анекдоти про проростання в домашніх умовах.
- 00:43:14 – Про температуру приготування та активність сульфорафану.
- 00:43:45 – Перетворення сульфорафану з глюкорафаніну кишковими бактеріями.
- 00:44:24 – Добавки працюють краще в поєднанні з активною мирозиназою з овочів.
- 00:44:56 – Техніка приготування та овочі хрестоцвітних.
- 00:46:06 – Ізотіоціанати як зоб.

Додаткова тема для обговорення: «Гострий біль у спині».
Біль у спині� є однією з найпоширеніших причин інвалідності та пропущених робочих днів у всьому світі. Біль у спині є другою за поширеністю причиною відвідувань лікаря, переважаючи лише інфекції верхніх дихальних шляхів. Приблизно 80 відсотків населення відчувають біль у спині хоча б раз у житті. Хребет – це складна структура, що складається з кісток, суглобів, зв’язок і м’язів, серед інших м’яких тканин. Травми та/або загострені стани, такі як �грижі диски, може зрештою призвести до симптомів болю в спині. Спортивні травми або травми в автомобільній катастрофі часто є найчастішою причиною болю в спині, однак іноді найпростіші рухи можуть мати хворобливі наслідки. На щастя, альтернативні варіанти лікування, такі як хіропрактика, можуть допомогти полегшити біль у спині за допомогою корекції хребта та ручних маніпуляцій, що в кінцевому підсумку покращує полегшення болю.
ЕКСТРА ДОДАТКО | ВАЖЛИВА ТЕМА: Рекомендований хіропрактик в Ель-Пасо, штат Техас
Інформація в цьому документі на "Які ризики надмірної експресії Nrf2?" не призначений для заміни особистих стосунків із кваліфікованим медичним працівником або ліцензованим лікарем і не є медичною консультацією. Ми заохочуємо вас приймати рішення щодо охорони здоров’я на основі ваших досліджень і партнерства з кваліфікованим медичним працівником.
Інформація в блозі та обговорення обсягу
Наша інформаційна сфера обмежується хіропрактикою, опорно-руховим апаратом, фізичними препаратами, оздоровленням, що сприяє етіологічному вісцеросоматичні порушення у клінічних презентаціях, клінічній динаміці асоційованого соматовісцерального рефлексу, комплексах підвивиху, чутливих питаннях здоров’я та/або статей, темах та дискусіях з функціональної медицини.
Надаємо та презентуємо клінічне співробітництво з фахівцями різних галузей. Кожен фахівець керується своєю професійною сферою практики та юрисдикцією ліцензування. Ми використовуємо протоколи функціонального здоров’я та оздоровлення для лікування та підтримки догляду за травмами або розладами опорно-рухового апарату.
Наші відео, дописи, теми, предмети та висновки охоплюють клінічні питання, проблеми та теми, які стосуються та прямо чи опосередковано підтримують нашу клінічну практику.*
Наш офіс обґрунтовано намагався надати підтверджувальні цитати та визначив відповідне дослідження або дослідження, що підтверджують наші публікації. За запитом ми надаємо копії допоміжних наукових досліджень, доступні регуляторним комісіям та громадськості.
Ми розуміємо, що ми розглядаємо питання, які потребують додаткового пояснення того, як це може допомогти в певному плані догляду або протоколі лікування; тому для подальшого обговорення вищезазначеної теми, будь ласка, не соромтеся запитувати Доктор Алекс Хіменес, округ Колумбія, Або зв'яжіться з нами за адресою 915-850-0900.
Ми тут, щоб допомогти вам та вашій родині.
Благословення
Д-р Алекс Хіменес Постійного струму, MSACP, RN*, CCST, IFMCP*, CIFM*, ATN*
електронна пошта: coach@elpasofunctionalmedicine.com
Ліцензія доктора хіропрактики (DC) у Техас & Нью-Мексико*
Техас, округ Колумбія, номер ліцензії TX5807, Нью-Мексико, округ Колумбія Номер ліцензії NM-DC2182
Ліцензія дипломованої медсестри (RN*) in Флорида
Ліцензія Флориди Ліцензія RN # RN9617241 (Контрольний номер 3558029)
Компактний статус: Мультидержавна ліцензія: Уповноважений на практику в Стани 40*
Доктор Алекс Хіменес, округ Колумбія, MSACP, RN* CIFM*, IFMCP*, ATN*, CCST
Моя цифрова візитна картка