Біохімія болю:Усі больові синдроми мають профіль запалення. Профіль запалення може відрізнятися від людини до людини, а також може відрізнятися у однієї людини в різний час. Лікування больових синдромів полягає в тому, щоб зрозуміти цей профіль запалення. Больові синдроми лікуються медикаментозним, хірургічним або обома. Метою є інгібування/придушення вироблення медіаторів запалення. І успішний результат - це той, який призводить до меншого запалення і, звичайно, меншого болю.
зміст
Біохімія болю
Цілі:
- Хто є ключовими гравцями
- Які біохімічні механізми?
- Які наслідки?
Огляд запалення:
Ключові гравці
 Чому болить плече? Огляд нейроанатомічної та біохімічної основи болю в плечі
Чому болить плече? Огляд нейроанатомічної та біохімічної основи болю в плечі
РЕЗЮМЕ
Якщо пацієнт запитає «чому у мене болить плече?», розмова швидко переходить до наукової теорії, а іноді й до необґрунтованих припущень. Часто клініцист усвідомлює межі наукової основи їх пояснення, демонструючи неповноту нашого розуміння природи болю в плечі. Цей огляд використовує систематичний підхід, щоб допомогти відповісти на фундаментальні питання, що стосуються болю в плечі, з метою надати уявлення про майбутні дослідження та нові методи лікування болю в плечі. Ми досліджуємо ролі (1) периферичних рецепторів, (2) обробки периферичного болю або «ноцицепції», (3) спинного мозку, (4) головного мозку, (5) розташування рецепторів у плечі та (6). ) нервова анатомія плеча. Ми також розглядаємо, як ці фактори можуть сприяти різницю клінічної картини, діагностики та лікування болю в плечі. Таким чином, ми прагнемо надати огляд складових частин периферичної системи виявлення болю та центральних механізмів обробки болю у плечі, які взаємодіють, викликаючи клінічний біль.
ВСТУП: ДУЖЕ КОРОТКА ІСТОРІЯ НАУКИ БОЛІ, ВАЖНА ДЛЯ КЛІНІЦІСТІВ
Природа болю, загалом, була предметом багатьох суперечок протягом останнього століття. У 17 столітті теорія Декарта 1 припускала, що інтенсивність болю безпосередньо пов’язана з кількістю пов’язаних з ними пошкоджень тканин і що біль обробляється одним особливим шляхом. Багато попередніх теорій спиралися на цю так звану «дуалістичну» філософію Декарта, розглядаючи біль як наслідок стимуляції «специфічного» периферичного больового рецептора в мозку. У 20 столітті почалася наукова боротьба між двома протилежними теоріями, а саме теорією специфічності та теорією зразків. Декартівська «теорія специфічності» розглядала біль як специфічну окрему модальність сенсорного введення з власним апаратом, тоді як «теорія шаблонів» вважала, що біль є результатом інтенсивної стимуляції неспецифічних рецепторів.2 У 1965 році Wall and Melzack 3 Теорія воріт болю надала докази моделі, в якій сприйняття болю модулювалося як сенсорним зворотним зв’язком, так і центральною нервовою системою. Інший величезний прогрес у теорії болю приблизно в той же час ознаменувався відкриттям специфічного способу дії опіоїдів.4 Згодом останні досягнення в області нейровізуалізації та молекулярної медицини значно розширили наше загальне розуміння болю.
Тож як це пов’язано з болем у плечі?�Біль у плечі є поширеною клінічною проблемою, і чітке розуміння того, як організм переробляє біль, є важливим для найкращої діагностики та лікування болю у пацієнта. Досягнення наших знань щодо обробки болю обіцяють пояснити невідповідність між патологією та сприйняттям болю, вони також можуть допомогти нам пояснити, чому деякі пацієнти не реагують на певні методи лікування.
ОСНОВНІ БУДІВНИКИ БОЛЮ
Периферичні сенсорні рецептори: механорецептор і «ноцицептор».
У кістково-м’язовій системі людини існує безліч типів периферичних сенсорних рецепторів. 5 Їх можна класифікувати на основі їхньої функції (як механорецептори, терморецептори або ноцицептори) або морфології (вільні нервові закінчення або різні типи інкапсульованих рецепторів).5 Потім різні типи рецепторів можуть бути додатково класифіковані на основі наявність певних хімічних маркерів. Наприклад, існують значні збіги між різними функціональними класами рецепторів
Обробка периферичного болю: «Ноцицепція».
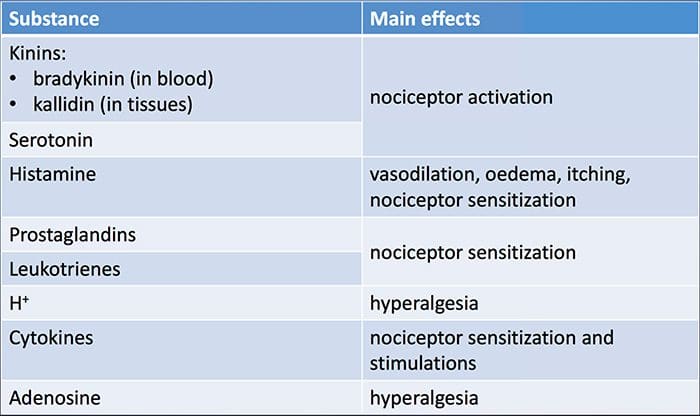
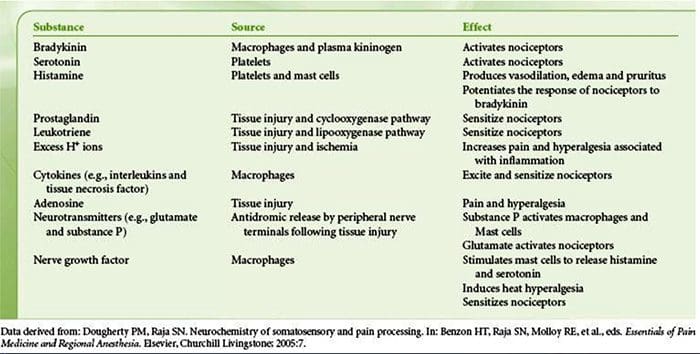
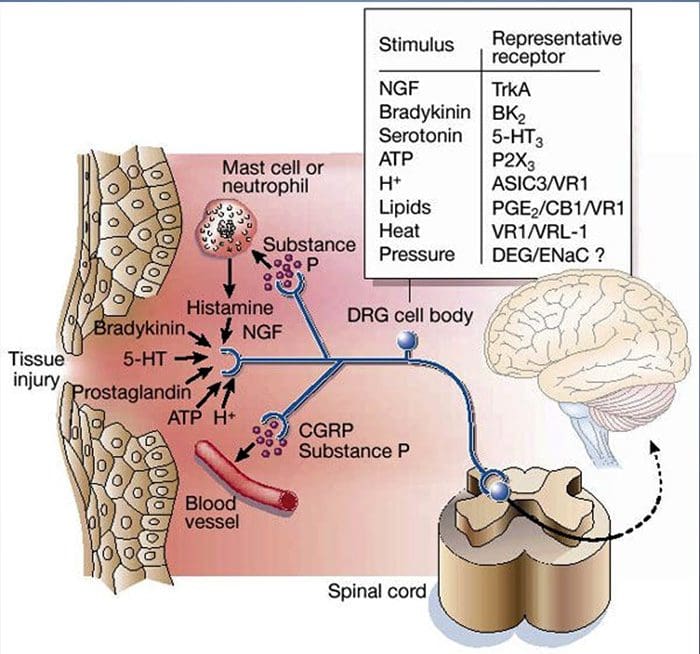
Пошкодження тканини включає в себе різноманітні медіатори запалення, які вивільняються пошкодженими клітинами, включаючи брадикінін, гістамін, 5-гідрокситриптамін, АТФ, оксид азоту та певні іони (K+ і H+). Активація шляху арахідонової кислоти призводить до вироблення простагландинів, тромбоксанів і лейкотрієнів. Цитокіни, включаючи інтерлейкіни та фактор некрозу пухлин α, і нейротрофіни, такі як фактор росту нервів (NGF), також вивільняються і беруть активну участь у полегшенні запалення.15 Інші речовини, такі як збудливі амінокислоти (глутамат) та опіоїди ( ендотелін-1) також були залучені до гострої запальної відповіді.16 17 Деякі з цих агентів можуть безпосередньо активувати ноцицептори, тоді як інші спричиняють залучення інших клітин, які потім вивільняють додаткові стимулюючі агенти.18 Цей локальний процес призводить до підвищення чутливості Ноцицептивних нейронів на їх нормальний вхід та/або залучення відповіді на нормальні підпорогові вхідні сигнали називають «периферичною сенсибілізацією». Рисунок 1 підсумовує деякі ключові механізми.
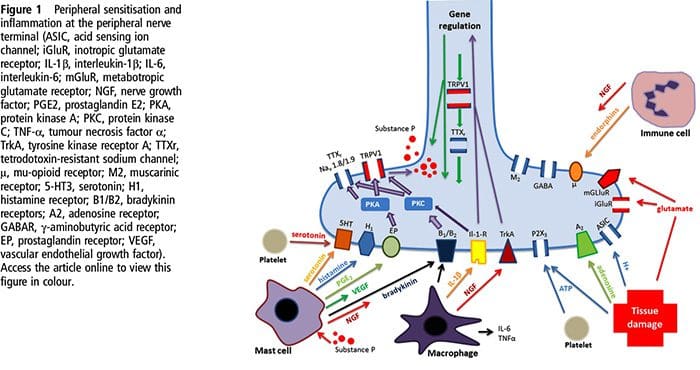 NGF і рецептор катіонного каналу з потенціальним рецептором підсімейства V члена 1 (TRPV1) мають симбіотичний зв’язок, коли справа доходить до запалення та сенсибілізації ноцирецепторів. Цитокіни, що виробляються в запаленій тканині, призводять до збільшення виробництва NGF.19 NGF стимулює вивільнення гістаміну і серотоніну (5-HT3) тучними клітинами, а також сенсибілізує ноцицептори, можливо, змінюючи властивості A? волокна таким чином, що більша їх частка стає ноцицептивною. Рецептор TRPV1 присутній у субпопуляції первинних аферентних волокон і активується капсаїцином, теплом і протонами. Рецептор TRPV1 синтезується в тілі клітини аферентного волокна і транспортується як до периферичних, так і до центральних терміналів, де він сприяє підвищенню чутливості ноцицептивних аферентів. Запалення призводить до вироблення NGF на периферії, який потім зв’язується з рецептором тирозинкінази типу 1 на терміналах ноцицептора, NGF потім транспортується в тіло клітини, де це призводить до посилення транскрипції TRPV1 і, отже, підвищення чутливості ноцицептора.19 20 NGF і інші медіатори запалення також сенсибілізують TRPV1 через різноманітний набір вторинних інформаційних шляхів. Вважається, що багато інших рецепторів, включаючи холінергічні рецептори, рецептори β-аміномасляної кислоти (ГАМК) і рецептори соматостатину, також беруть участь у чутливості периферичних ноцицепторів.
NGF і рецептор катіонного каналу з потенціальним рецептором підсімейства V члена 1 (TRPV1) мають симбіотичний зв’язок, коли справа доходить до запалення та сенсибілізації ноцирецепторів. Цитокіни, що виробляються в запаленій тканині, призводять до збільшення виробництва NGF.19 NGF стимулює вивільнення гістаміну і серотоніну (5-HT3) тучними клітинами, а також сенсибілізує ноцицептори, можливо, змінюючи властивості A? волокна таким чином, що більша їх частка стає ноцицептивною. Рецептор TRPV1 присутній у субпопуляції первинних аферентних волокон і активується капсаїцином, теплом і протонами. Рецептор TRPV1 синтезується в тілі клітини аферентного волокна і транспортується як до периферичних, так і до центральних терміналів, де він сприяє підвищенню чутливості ноцицептивних аферентів. Запалення призводить до вироблення NGF на периферії, який потім зв’язується з рецептором тирозинкінази типу 1 на терміналах ноцицептора, NGF потім транспортується в тіло клітини, де це призводить до посилення транскрипції TRPV1 і, отже, підвищення чутливості ноцицептора.19 20 NGF і інші медіатори запалення також сенсибілізують TRPV1 через різноманітний набір вторинних інформаційних шляхів. Вважається, що багато інших рецепторів, включаючи холінергічні рецептори, рецептори β-аміномасляної кислоти (ГАМК) і рецептори соматостатину, також беруть участь у чутливості периферичних ноцицепторів.
Велика кількість медіаторів запалення була спеціально залучена до болю в плечі та захворювання ротаторної манжети манжети.21�25 Хоча деякі хімічні медіатори безпосередньо активують ноцицептори, більшість з них призводять до змін у самому сенсорному нейроні, а не безпосередньо його активації. Ці зміни можуть залежати від ранньої посттрансляційної або відстроченої транскрипції. Прикладами першого є зміни в рецепторі TRPV1 або в напругозалежних іонних каналах, які є результатом фосфорилювання пов’язаних з мембраною білків. Приклади останнього включають індукований NGF збільшення продукції каналу TRV1 та індуковану кальцієм активацію внутрішньоклітинних факторів транскрипції.
Молекулярні механізми ноцицепції
Відчуття болю попереджає нас про реальну або наближається травму і викликає відповідні захисні реакції. На жаль, біль часто доживає своєї корисності як система попередження і натомість стає хронічною та виснажливою. Цей перехід до хронічної фази включає зміни в спинному і головному мозку, але існує також чудова модуляція, коли повідомлення про біль ініціюються – на рівні первинного сенсорного нейрона. Зусилля визначити, як ці нейрони виявляють подразники, що викликають біль теплового, механічного або хімічного характеру, відкрили нові механізми передачі сигналів і наблизили нас до розуміння молекулярних подій, які сприяють переходу від гострого болю до постійного.
 Нейрохімія ноцицепторів
Нейрохімія ноцицепторів
Глутамат є переважаючим збудливим нейромедіатором у всіх ноцицепторах. Проте гістохімічні дослідження DRG дорослих виявляють два широкі класи немієлінізованих C волокон.
Хімічні датчики для посилення болю
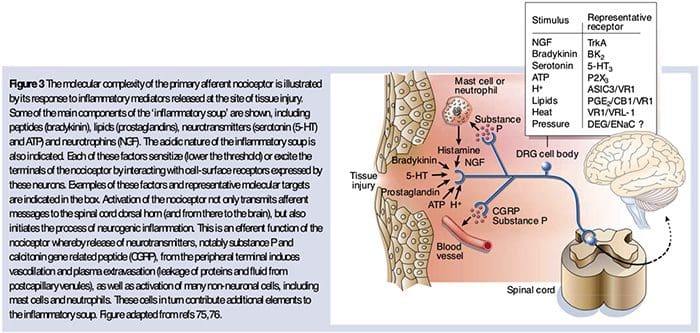
Як описано вище, травма посилює наш біль, підвищуючи чутливість ноцицепторів як до теплових, так і до механічних подразників. Це явище частково є результатом виробництва та вивільнення хімічних медіаторів із первинного сенсорного термінала та з ненейронних клітин (наприклад, фібробластів, тучних клітин, нейтрофілів і тромбоцитів) у навколишнє середовище36 (рис. 3). Деякі компоненти запального супу (наприклад, протони, АТФ, серотонін або ліпіди) можуть змінювати збудливість нейронів безпосередньо, взаємодіючи з іонними каналами на поверхні ноцицептора, тоді як інші (наприклад, брадикінін і NGF) зв’язуються з метаботропними рецепторами і опосередковують свої ефекти через сигнальні каскади другого месенджера11. Значний прогрес був досягнутий у розумінні біохімічних основ таких модулюючих механізмів.
Позаклітинні протони та ацидоз тканин
Місцевий ацидоз тканин є характерною фізіологічною реакцією на травму, і ступінь пов’язаного з цим болю чи дискомфорту добре корелює із величиною закислення37. Нанесення кислоти (рН 5) на шкіру викликає тривалі розряди в третині або більше полімодальних ноцицепторів, які іннервують рецепторне поле 20.
 Клітинні та молекулярні механізми болю
Клітинні та молекулярні механізми болю
абстрактний
Нервова система виявляє та інтерпретує широкий спектр теплових і механічних подразників, а також зовнішні та ендогенні хімічні подразники. Коли вони інтенсивні, ці стимули викликають гострий біль, а в умовах стійкої травми компоненти периферичної та центральної нервової системи шляху передачі болю виявляють величезну пластичність, посилюючи больові сигнали та викликаючи гіперчутливість. Коли пластичність сприяє захисним рефлексам, це може бути корисно, але коли зміни зберігаються, може виникнути хронічний больовий стан. Генетичні, електрофізіологічні та фармакологічні дослідження з’ясовують молекулярні механізми, які лежать в основі виявлення, кодування та модуляції шкідливих подразників, які викликають біль.
Вступ: гострий і постійний біль
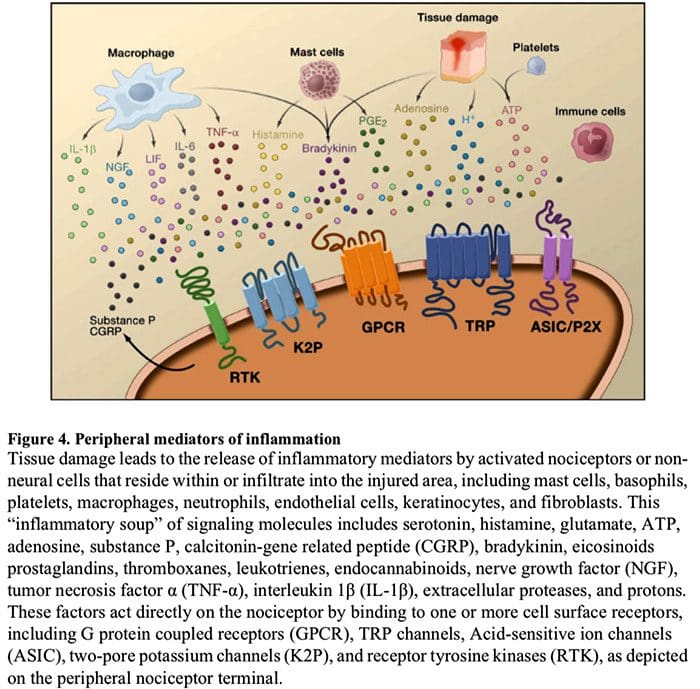
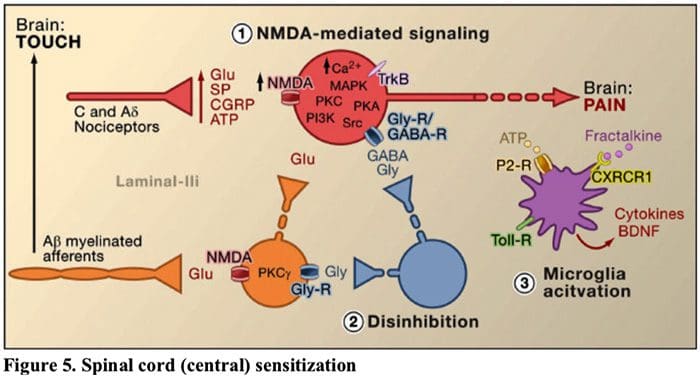 Малюнок 5. Сенсибілізація спинного мозку (центральна).
Малюнок 5. Сенсибілізація спинного мозку (центральна).
- Сенсибілізація, опосередкована рецептором глутамат/NMDA.�Після інтенсивної стимуляції або тривалої травми активовані C і A? ноцицептори вивільняють різноманітні нейромедіатори, включаючи лутамат, речовину P, пептид, пов’язаний з геном кальцитоніну (CGRP) і АТФ, на вихідні нейрони в пластинці I поверхневого спинного рогу (червоний). Як наслідок, зазвичай тихі глутаматні рецептори NMDA, розташовані в постсинаптичному нейроні, тепер можуть сигналізувати, збільшувати внутрішньоклітинний кальцій і активувати безліч кальцій-залежних сигнальних шляхів і вторинних месенджерів, включаючи мітоген-активовану протеїнкіназу (MAPK), протеїнкіназу C (PKC). , протеїнкіназа А (PKA) і Src. Цей каскад подій підвищить збудливість вихідного нейрона і полегшить передачу больових повідомлень до мозку.
- Розгальмованість.За звичайних обставин гальмівні інтернейрони (сині) постійно вивільняють ГАМК та/або гліцин (Gly), щоб зменшити збудливість вихідних нейронів пластинки I та модулювати передачу болю (гальмівний тон). Проте в умовах травми це гальмування може бути втрачено, що призводить до гіпералгезії. Крім того, розгальмування може уможливити неноцицептивний мієліновий A? первинні аференти, щоб задіяти схему передачі болю так, що зазвичай нешкідливі подразники тепер сприймаються як болючі. Частково це відбувається через розгальмування збудливої PKC? експресують інтернейрони у внутрішній пластинці II.
- Активація мікроглії.Ураження периферичних нервів сприяє вивільненню АТФ і хемокінового фрактакіну, які стимулюють клітини мікроглії. Зокрема, активація пуринергічних, CX3CR1 і Toll-подібних рецепторів на мікроглії (фіолетовий) призводить до вивільнення нейротрофічного фактора головного мозку (BDNF), який через активацію рецепторів TrkB, що експресуються нейронами, що виводять пластинку I, сприяє підвищенню збудливості та посилення болю у відповідь як на шкідливу, так і на нешкідливу стимуляцію (тобто гіпералгезію та алодинію). Активована мікроглія також вивільняє безліч цитокінів, таких як фактор некрозу пухлини ? (ФНП?), інтерлейкін-1? і 6 (IL-1?, IL-6) та інші фактори, що сприяють центральній сенсибілізації.
Хімічна середовище запалення
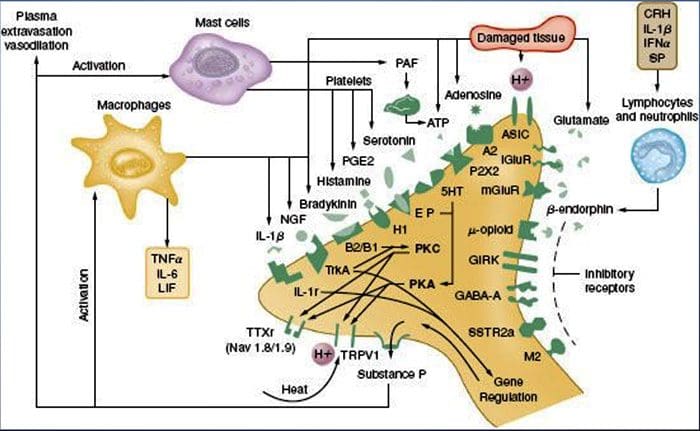
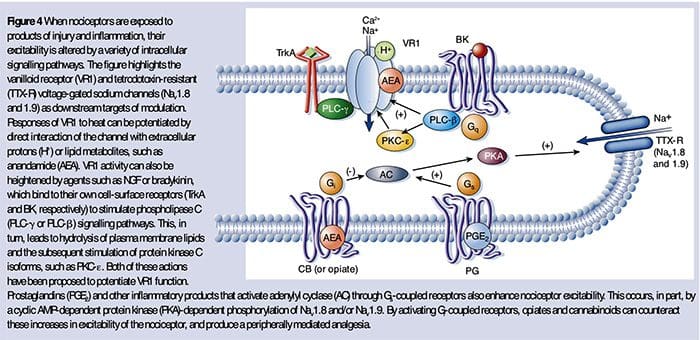
Периферична сенсибілізація частіше виникає внаслідок пов’язаних із запаленням змін у хімічному середовищі нервового волокна (McMahon et al., 2008). Таким чином, пошкодження тканини часто супроводжується накопиченням ендогенних факторів, що вивільняються з активованих ноцицепторів або ненейральних клітин, які знаходяться всередині або інфільтруються в пошкодженій області (включаючи тучні клітини, базофіли, тромбоцити, макрофаги, нейтрофіли, ендотеліальні клітини, кератиноцити та фібробласти). Колективно. ці фактори, які називають «запальним супом», представляють широкий спектр сигнальних молекул, включаючи нейромедіатори, пептиди (речовина P, CGRP, брадикінін), ейкозиноїди та споріднені ліпіди (простагландини, тромбоксани, лейкотрієни, ендоканабініноїди, нейроканнабіноїди, , і хемокіни, а також позаклітинні протеази і протони. Примітно, що ноцицептори експресують один або кілька рецепторів клітинної поверхні, здатних розпізнавати і реагувати на кожен із цих прозапальних або про-алгетичних агентів (Малюнок 4). Такі взаємодії посилюють збудливість нервового волокна, тим самим підвищуючи його чутливість до температури або дотику.
Безсумнівно, найпоширеніший підхід до зменшення запального болю включає пригнічення синтезу або накопичення компонентів запального супу. Найкращим прикладом цього є нестероїдні протизапальні препарати, такі як аспірин або ібупрофен, які зменшують запальний біль і гіпералгезію, пригнічуючи циклооксигенази (ЦОГ-1 і ЦОГ-2), що беруть участь у синтезі простагландинів. Другий підхід полягає в блокуванні дії агентів запалення на ноцицептор. Тут ми виділяємо приклади, які дають нове уявлення про клітинні механізми периферичної сенсибілізації або які є основою нових терапевтичних стратегій для лікування запального болю.
NGF, можливо, найбільш відомий своєю роллю нейротрофічного фактора, необхідного для виживання та розвитку сенсорних нейронів під час ембріогенезу, але у дорослих NGF також виробляється при пошкодженні тканин і є важливим компонентом запального супу (Ritner et. ін., 2009). Серед багатьох клітинних мішеней NGF діє безпосередньо на пептидергічні ноцицептори волокна C, які експресують тирозинкіназу рецептора NGF з високою афінністю, TrkA, а також низькоафінний нейротрофіновий рецептор p75 (Chao, 2003; Snider and McMahon, 1998). NGF викликає глибоку гіперчутливість до тепла та механічних подразників за допомогою двох тимчасових механізмів. Спочатку взаємодія NGF-TrkA активує низхідні сигнальні шляхи, включаючи фосфоліпазу C (PLC), мітоген-активовану протеїнкіназу (MAPK) і фосфоінозитид-3-кіназу (PI3K). Це призводить до функціонального посилення цільових білків на периферійному терміналі ноцицептора, особливо TRPV1, що призводить до швидкої зміни клітинної та поведінкової чутливості до тепла (Chuang et al., 2001).
Незалежно від їх проноцицептивних механізмів, перешкоджання передачі сигналів нейротрофіну або цитокінам стало основною стратегією контролю запального захворювання або болю, що виникає. Основний підхід передбачає блокування NGF або TNF-? дію з нейтралізуючими антитілами. У випадку TNF-?, це було надзвичайно ефективним у лікуванні численних аутоімунних захворювань, включаючи ревматоїдний артрит, що призвело до різкого зниження як руйнування тканин, так і супроводжуючої гіпералгезії (Atzeni et al., 2005). Оскільки основна дія NGF на дорослий ноцицептор відбувається на фоні запалення, перевага цього підходу полягає в тому, що гіпералгезія зменшується, не впливаючи на нормальне сприйняття болю. Справді, антитіла проти NGF зараз проходять клінічні випробування для лікування запальних больових синдромів (Hefti et al., 2006).
Сенсибілізація, опосередкована глутаматом/NMDA-рецептором
Гострий біль сигналізується вивільненням глутамату з центральних терміналів ноцицепторів, що генерує збудливі постсинаптичні струми (EPSC) у нейронах спинного рогу другого порядку. Це відбувається насамперед через активацію постсинаптичних АМРА і каїнатних підтипів іонотропних глутаматних рецепторів. Підсумування підпорогових EPSC в постсинаптичному нейроні в кінцевому підсумку призведе до запуску потенціалу дії та передачі больового повідомлення нейронам вищого порядку.
Інші дослідження показують, що зміни в проекційному нейроні самі по собі сприяють гальмівному процесу. Наприклад, ушкодження периферичних нервів значно погіршує регуляцію K+- Cl- ко-транспортера KCC2, який є важливим для підтримки нормальних градієнтів K+ і Cl- через плазматичні мембрани (Coull et al., 2003). Зниження регуляції KCC2, яка експресується в нейронах проекції пластинки I, призводить до зсуву в градієнті Cl, таким чином, що активація рецепторів GABA-A деполяризує, а не гіперполяризує нейрони проекції пластинки I. Це, в свою чергу, підвищить збудливість і посилить передачу болю. Дійсно, фармакологічна блокада або опосередкована siRNA зниження регуляції KCC2 у щурів викликає механічну алодинію.
джерела:
Чому болить плече? Огляд нейроанатомічних та біохімічних основ болю в плечі
Бенджамін Джон Флойд Дін, Стівен Едвард Гвілім, Ендрю Джонатан Карр
Клітинні та молекулярні механізми болю
Аллан І. Басбаум1, Діана М. Баутіста2, Грегорі Шеррер1 та Девід Джуліус3
1 Кафедра анатомії, Каліфорнійський університет, Сан-Франциско 94158
2 Кафедра молекулярної та клітинної біології Каліфорнійського університету, Берклі, Каліфорнія 94720 3 Кафедра фізіології Каліфорнійського університету, Сан-Франциско 94158
Молекулярні механізми ноцицепції
Девід Джуліус* та Аллан І. Басбаум
*Кафедра клітинної та молекулярної фармакології, кафедри анатомії та фізіології та Центр інтегративної нейронауки Фонду WM Keck, Каліфорнійський університет Сан-Франциско, Сан-Франциско, Каліфорнія 94143, США (електронна пошта: julius@socrates.ucsf.edu)
Інформація в цьому документі на "Біохімія болю" не призначений для заміни особистих стосунків із кваліфікованим медичним працівником або ліцензованим лікарем і не є медичною консультацією. Ми заохочуємо вас приймати рішення щодо охорони здоров’я на основі ваших досліджень і партнерства з кваліфікованим медичним працівником.
Інформація в блозі та обговорення обсягу
Наша інформаційна сфера обмежується хіропрактикою, опорно-руховим апаратом, фізичними препаратами, оздоровленням, що сприяє етіологічному вісцеросоматичні порушення у клінічних презентаціях, клінічній динаміці асоційованого соматовісцерального рефлексу, комплексах підвивиху, чутливих питаннях здоров’я та/або статей, темах та дискусіях з функціональної медицини.
Надаємо та презентуємо клінічне співробітництво з фахівцями різних галузей. Кожен фахівець керується своєю професійною сферою практики та юрисдикцією ліцензування. Ми використовуємо протоколи функціонального здоров’я та оздоровлення для лікування та підтримки догляду за травмами або розладами опорно-рухового апарату.
Наші відео, дописи, теми, предмети та висновки охоплюють клінічні питання, проблеми та теми, які стосуються та прямо чи опосередковано підтримують нашу клінічну практику.*
Наш офіс обґрунтовано намагався надати підтверджувальні цитати та визначив відповідне дослідження або дослідження, що підтверджують наші публікації. За запитом ми надаємо копії допоміжних наукових досліджень, доступні регуляторним комісіям та громадськості.
Ми розуміємо, що ми розглядаємо питання, які потребують додаткового пояснення того, як це може допомогти в певному плані догляду або протоколі лікування; тому для подальшого обговорення вищезазначеної теми, будь ласка, не соромтеся запитувати Доктор Алекс Хіменес, округ Колумбія, Або зв'яжіться з нами за адресою 915-850-0900.
Ми тут, щоб допомогти вам та вашій родині.
Благословення
Д-р Алекс Хіменес Постійного струму, MSACP, RN*, CCST, IFMCP*, CIFM*, ATN*
електронна пошта: coach@elpasofunctionalmedicine.com
Ліцензія доктора хіропрактики (DC) у Техас & Нью-Мексико*
Техас, округ Колумбія, номер ліцензії TX5807, Нью-Мексико, округ Колумбія Номер ліцензії NM-DC2182
Ліцензія дипломованої медсестри (RN*) in Флорида
Ліцензія Флориди Ліцензія RN # RN9617241 (Контрольний номер 3558029)
Компактний статус: Мультидержавна ліцензія: Уповноважений на практику в Стани 40*
Доктор Алекс Хіменес, округ Колумбія, MSACP, RN* CIFM*, IFMCP*, ATN*, CCST
Моя цифрова візитна картка







