У дитинстві всіх нас вчили, що є 5 органів чуття: зір, смак, звук, нюх і дотик. Початкові чотири органи почуттів використовують чіткі, чіткі органи, такі як очі, смакові рецептори, вуха та ніс, але як саме відчуття тіла впливає на дотик? Дотик відчувається по всьому тілу, як всередині, так і зовні. Немає жодного окремого органу, який відповідає за відчуття дотику. Навпаки, навколо всього тіла є крихітні рецептори або нервові закінчення, які відчувають дотик там, де це відбувається, і посилає сигнали в мозок з інформацією про тип дотику, який відбувся. Оскільки смакова сосочка на язиці розпізнає смак, механорецептори — це залози в шкірі та інших органах, які виявляють відчуття дотику. Вони відомі як механорецепторы оскільки вони розроблені для виявлення механічних відчуттів або різниці в тиску.
зміст
Роль механорецепторів
Людина розуміє, що вона відчула відчуття, коли орган, відповідальний за виявлення цього певного відчуття, надсилає повідомлення в мозок, який є основним органом, який обробляє та впорядковує всю інформацію. Повідомлення надсилаються з усіх частин тіла до мозку через дроти, які називаються нейронами. Існують тисячі маленьких нейронів, які розгалужуються до всіх ділянок людського тіла, і на закінченнях багатьох із цих нейронів є механорецептори. Щоб продемонструвати, що відбувається, коли ви торкаєтеся об’єкта, ми використаємо приклад.
Уявіть собі, як на вашу руку впаде комар. Стим цієї комахи, такий легкий, стимулює механорецептори в цій конкретній ділянці руки. Ці механорецептори надсилають повідомлення по нейрону, з яким вони підключені. Нейрон з’єднується аж до мозку, який отримує повідомлення про те, що щось торкається вашого тіла в точному місці конкретного механорецептора, який надіслав повідомлення. Мозок буде діяти з цією порадою. Можливо, це підкаже очам подивитися на область руки, яка виявила підпис. І коли очі повідомляють мозку, що на руці є комар, мозок може наказати руці швидко відмахнути його. Так працюють механорецептори. Метою статті нижче є продемонструвати, а також детально обговорити функціональну організацію та молекулярні детермінанти механорецепторів.
Чуття дотику: функціональна організація та молекулярні детермінанти механочутливих рецепторів
абстрактний
Шкірні механорецептори локалізуються в різних шарах шкіри, де вони виявляють широкий спектр механічних подразників, включаючи легкий кисть, розтягування, вібрацію та шкідливий тиск. Ця різноманітність стимулів узгоджується з різноманітним набором спеціалізованих механорецепторів, які специфічним чином реагують на деформацію шкіри та передають ці стимули до вищих структур мозку. Дослідження механорецепторів і генетично піддаються чутливості нервових закінчень починають відкривати механізми дотику. Робота в цій області надала дослідникам більш глибоке розуміння організації ланцюга, що лежить в основі сприйняття дотику. Нові іонні канали з’явилися як кандидати на молекули трансдукції, а властивості механічно керованих струмів покращили наше розуміння механізмів адаптації до тактильних подразників. Цей огляд висвітлює прогрес, досягнутий у характеристиці функціональних властивостей механорецепторів у волосистій та голій шкірі та іонних каналів, які виявляють механічні дії та адаптацію механорецепторів до форми.
Ключові слова: механорецептор, механочутливий канал, біль, шкіра, соматосенсорна система, дотик
Вступ
Дотик – це виявлення механічних подразників, що впливають на шкіру, включаючи нешкідливі та шкідливі механічні подразники. Це важливе відчуття для виживання та розвитку ссавців і людини. Контакт твердих предметів і рідин зі шкірою дає необхідну інформацію центральній нервовій системі, що дозволяє досліджувати і розпізнавати навколишнє середовище і ініціює рух або запланований рух руки. Дотик також дуже важливий для учнівства, соціальних контактів і сексуальності. Дотик є найменш вразливим почуттям, хоча воно може бути спотворене (гіперестезія, гіпестезія) при багатьох патологічних станах.1-3
Відповіді на дотик передбачають дуже точне кодування механічної інформації. Шкірні механорецептори локалізуються в різних шарах шкіри, де вони виявляють широкий спектр механічних подразників, включаючи легкий щіткою, розтягування, вібрацію, відхилення волосся і шкідливий тиск. Ця різноманітність стимулів узгоджується з різноманітним набором спеціалізованих механорецепторів, які специфічним чином реагують на деформацію шкіри та передають ці стимули до вищих структур мозку. Соматосенсорні нейрони шкіри діляться на дві групи: низькопорогові механорецептори (LTMR), які реагують на доброякісний тиск, і високопорогові механорецептори (HTMR), які реагують на шкідливу механічну стимуляцію. Тіла клітин LTMR і HTMR знаходяться в гангліях дорсального корінця (DRG) і краніальних сенсорних гангліях (трійчастих гангліях). Нервові волокна, пов’язані з LTMR і HTMR, класифікуються як A?-, A?- або C-волокна на основі їхньої швидкості проведення потенціалу дії. Волокна C немієлінізовані і мають найнижчу швидкість провідності (~2 м/с), тоді як A? і А? волокна слабо і сильно мієлінізовані, демонструючи проміжну (~12 м/с) і швидку (~20 м/с) швидкість провідності відповідно. LTMR також класифікуються як реакції з повільною або швидкою адаптацією (SA- та RA-LTMR) відповідно до їхньої швидкості адаптації до тривалого механічного стимулу. Крім того, вони відрізняються шкірними кінцевими органами, які вони іннервують, і бажаними подразниками.
Здатність механорецепторів виявляти механічні сигнали залежить від наявності іонних каналів механопреобразователей, які швидко перетворюють механічні сили в електричні сигнали та деполяризують рецепторне поле. Ця локальна деполяризація, яка називається рецепторним потенціалом, може генерувати потенціали дії, які поширюються до центральної нервової системи. Однак властивості молекул, які опосередковують механотрансдукцію та адаптацію до механічних сил, залишаються неясними.
У цьому огляді ми надаємо огляд властивостей механорецепторів ссавців у нешкідливому та шкідливому дотику до волохатої та голої шкіри. Ми також розглядаємо останні знання про властивості механічно-керованих струмів, намагаючись пояснити механізм адаптації механорецепторів. Нарешті, ми розглядаємо останній прогрес, досягнутий у визначенні іонних каналів і пов’язаних з ними білків, відповідальних за генерацію механокерованих струмів.
Нешкідливий дотик
LTMR, пов’язані з волосяними фолікулами
Волосяні фолікули являють собою міні-органи, що виробляють волосяний стрижень, які розпізнають легкий дотик. Волокна, пов’язані з волосяними фолікулами, реагують на рух волосся та його напрямок, запускаючи потяги потенціалів дії при появі та видаленні подразника. Вони швидко адаптуються до рецепторів.
Кішка і кролик. У шерсті кішок і кроликів волосяні фолікули можна розділити на три типи волосяних фолікулів: пуховий, гвардійський і тілотріх. Пухові волоски (підшерсть, шерсть, пушкові)4 є найчисельнішими, найкоротшими і найтоншими волосками шерсті. Вони хвилясті, безбарвні і виходять групами по два-чотири волоски із загального отвору на шкірі. Гвардійські волоски (монотріхи, підсвічники, топери)4 злегка вигнуті, пігментовані або непігментовані, і виходять поодинці з гирла їх фолікулів. Тилотрихи найменш численні, найдовші та найтовстіші волоски.5,6 Вони пігментовані або непігментовані, іноді обидва і виходять окремо з фолікула, який оточений петлею капілярних кровоносних судин. Сенсорні волокна, які живлять волосяний фолікул, розташовані нижче сальної залози і належать до A? або волокна A?-LTMR.7
У тісному приляганні до нижнього стрижня волосся, трохи нижче рівня сальної залози розташоване кільце ланцетних закінчень ворсинки Руффіні. Ці чутливі нервові закінчення розташовані по спіралі навколо волосини в сполучній тканині, яка утворює волосяний фолікул. У волосяному фолікулі також є вільні нервові закінчення, деякі з них утворюють механорецептори. Часто дотикові тільця (див. гола шкіра) оточують область шийки тилотрихового фолікула.
Властивості мієлінових нервових закінчень волохатої шкіри кішок і кроликів інтенсивно досліджували в період 1930–1970 років (огляд у Hamann, 1995).8 Примітно, що Браун і Ігго вивчали 772 одиниці з мієліновими аферентними нервовими волокнами в підшкірних нервах кішки. та кролика, класифікували реакції за трьома типами рецепторів, що відповідають руху волосків Down (рецептори типу D), волосся Guard (рецептори типу G) і волосся Tylotrich (рецептори типу T).9 Усі реакції аферентних нервових волокон були зібрані разом. у рецепторі типу I (RA I), що швидко адаптується, протиставляючи рецептору Пачініа під назвою RA II. Механорецептори RA I визначають швидкість механічного подразника і мають різку межу. Вони не виявляють температурних змін. Берджесс та ін. також описав польовий рецептор, який швидко адаптується, який оптимально реагує на погладжування шкіри або рух кількох волосків, що було приписано стимуляції закінчень піло-Руффіні. Жодна реакція волосяного фолікула не була пов'язана з активністю волокна С.10
Миші У дорсальній волосяній шкірі мишей описано три основних типи волосяних фолікулів: зигзагоподібні (близько 72%), шило/шило (близько 23%) і щиткові або тилотрихові (близько 5%).11-14 Зигзаг і шило/ Волосяні фолікули auchenne утворюють тонші та коротші волосяні стрижні та пов’язані з однією сальною залозою. Захисні або тилотрихові волоски є найдовшими з типів волосяних фолікулів. Для них характерна велика волосяна цибулина, пов’язана з двома сальними залозами. Волосся з щитком і шилом/ашеном розташовані в ітераційному порядку з регулярними відстанями, тоді як зигзагоподібні волоски густо заселяють ділянки шкіри, що оточують два більші типи волосяних фолікулів (рис. 1 (A1, A2 і A3)].
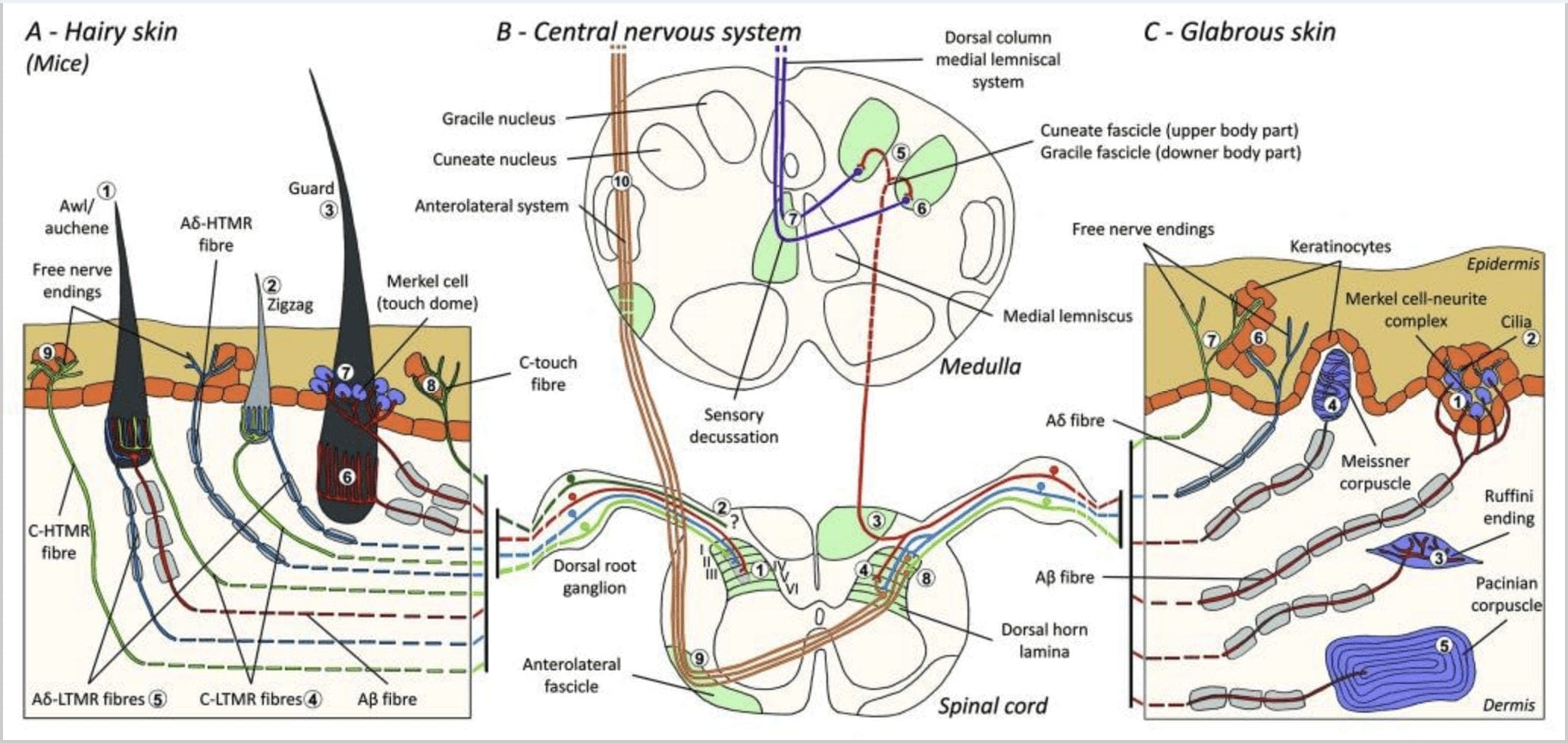
Малюнок 1. Організація та проекції шкірних механорецепторів. У волосистій шкірі легкий щіточок і дотик в основному виявляються по іннервації навколо волосяних фолікулів: шило/ошень (A1), зигзагоподібний (A2) і щиток (A3). Волосся шило/ошень тричі іннервуються ланцетними закінченнями C-LTMR (A4), A?-LTMR і A? швидко адаптується-LTMR (A6). Зигзагоподібні волосяні фолікули є коротшими волосяними стрижнями і іннервуються як C-LTMR (A4), так і A? -LTMR ланцетні закінчення (A5). Найдовші захисні волосяні фолікули іннервуються А? швидко адаптуються-LTMR поздовжні ланцетні закінчення (A6) і пов'язані з A? повільна адаптація-LTMR закінчень сенсорного купола (A7). Центральні виступи всіх цих волокон закінчуються окремими, але частково перекриваються пластинками спинного рогу спинного мозку (C-LTMR в пластинці II, A?-LTMR в пластинці III і A?-LTMR в пластинках IV і V). Проекції LTMR, які іннервують ті самі або сусідні волосяні фолікули, вирівняні, щоб утворити вузький стовпчик у спинному розі спинного мозку (B1 сірий колір). Лише в волосистій шкірі субпопуляція вільних закінчень С-волокон іннервує епідерміс і реагує на приємний дотик (A8). Ці волокна C-touch не реагують на шкідливий дотик, і їхнє проходження ще не відоме (B2). У голій шкірі нешкідливий дотик опосередковується чотирма типами LTMR. Клітинно-невритний комплекс Меркеля знаходиться в базальному шарі епідермісу (С1). Цей механорецептор складається з розташування між багатьма клітинами Меркеля та збільшеним нервовим закінченням з одного A? клітковина. Клітини Меркеля мають пальцеподібні відростки, що контактують з кератиноцитами (С2). Закінчення Руффіні локалізується в дермі. Це тонкі сигароподібні інкапсульовані сенсорні закінчення, з'єднані з A? волокно (С3). Телець Мейснера, пов'язаний з A? нервове закінчення і знаходиться в шкірних сосочках. Цей інкапсульований механорецептор складається з упакованих підтримуючих клітин, розташованих у вигляді горизонтальних пластин, оточених сполучною тканиною (С4). Тельце Пачіна є більш глибоким механорецептором. Один єдиний А? Немієлінові нервові закінчення закінчуються в центрі цього великого яйцевидного тільця, що складається з концентричних пластинок. Проекції цих волокон A?-LTMR у спинному мозку поділяються на дві гілки. Головна центральна гілка (B3) піднімається в спинному мозку в іпсилатеральній дорсальній частині, утворюючи клиновидні або грацильні пучки (B5) на рівні мозкового речовини, де первинні аференти утворюють свій перший синапс (B6). Вторинні нейрони здійснюють сенсорний перехрест (B7), щоб утворити тракт на медіальному лемніску, який піднімається через стовбур мозку до середнього мозку, зокрема в таламус. Вторинна гілка LTMR закінчується в дорсальному розі в пластинках II, IV, V і заважає передачі болю (B4). Шкідливий дотик визначається вільним нервовим закінченням в епідермісі як волосистої (A9), так і голої шкіри (C7). Ці механорецептори є закінченням A?-HTMR і C-HTMR в тісному контакті з сусідніми кератиноцитами (C6). A?-hTMR закінчується в пластинках I і V; C-HTMR закінчується в пластинках I і II (B8). На рівні дорсальних рогів спинного мозку первинні аферентні HTMR утворюють синапси з вторинними нейронами, які перетинають середню лінію і піднімаються до вищої структури мозку в передньо-латеральному пучку (B9, B10).
Нещодавно Джінті та його співробітники використали комбінацію підходів молекулярно-генетичного маркування та соматотопічного ретроградного відстеження для візуалізації організації периферичних і центральних аксональних закінчень LTMR у мишей.15 Їхні висновки підтверджують модель, в якій індивідуальні особливості складного тактильного стимулу є витягується трьома типами волосяних фолікулів і передається за допомогою унікальних комбінацій волокон A?-, A?- і C- до спинного рогу.
Вони показали, що генетичне маркування нейронів DRG, позитивних на тирозин гідроксилазу (TH+), характеризує популяцію непептидергічних сенсорних нейронів малого діаметра і дозволяє візуалізувати периферичні закінчення C-LTMR в шкірі. Як не дивно, було виявлено, що аксональні гілки окремих C-LTMR утворяться і утворюють поздовжні ланцетні закінчення, які тісно пов’язані з зигзагом (80% закінчень) і шилом/аушеном (20% закінчень), але не тилотритними волосяними фолікулами [рис. 1 (A4)]. Довгий час вважалося, що поздовжні ланцетні закінчення належать виключно до A?-LTMR, і тому було неочікувано, що закінчення C-LTMR утворять поздовжні ланцетні закінчення.15 Ці C-LTMR мають проміжну адаптацію в порівнянні з повільно та швидко адаптованими мієлінові механорецептори [рис. 2 (C1)].
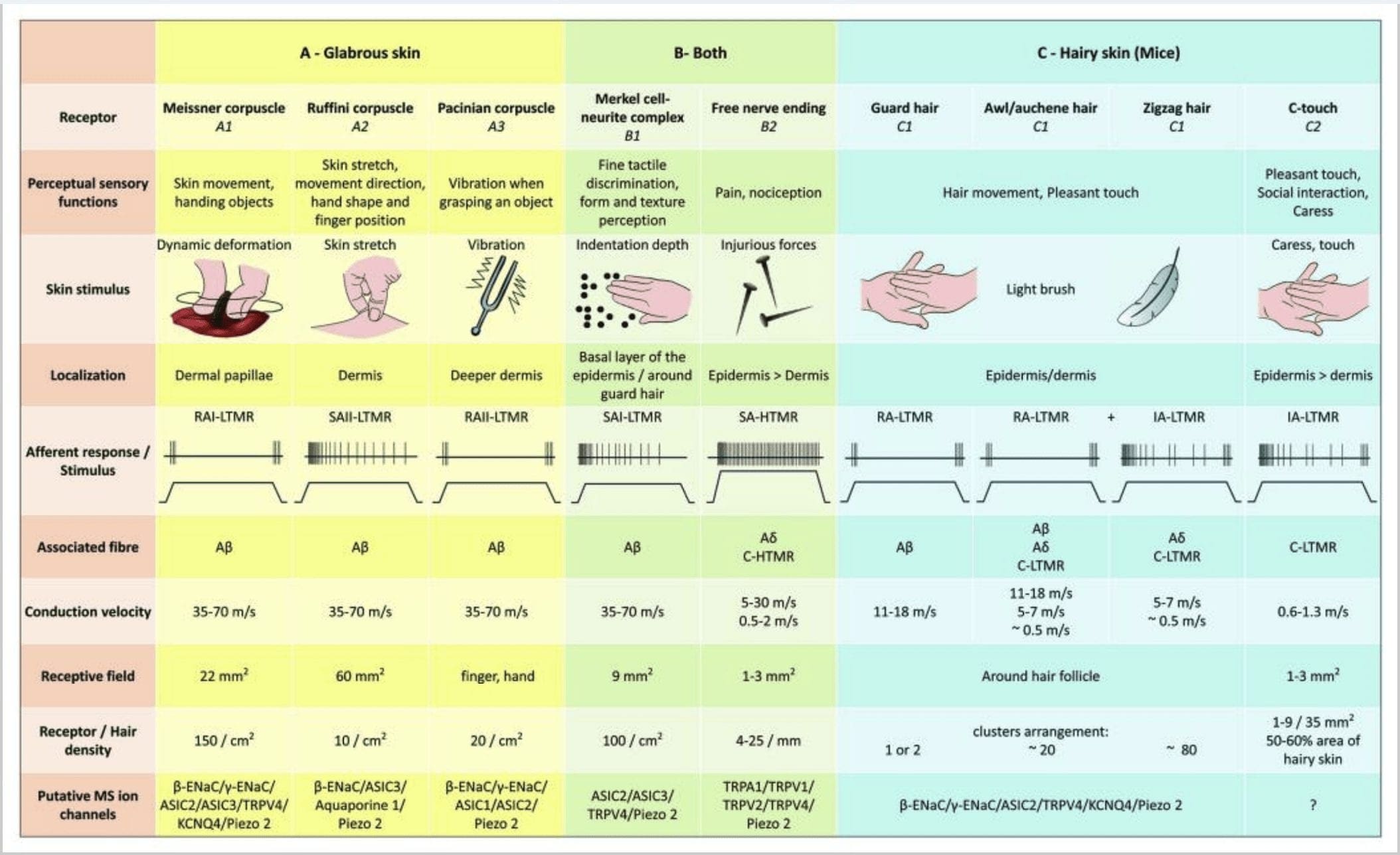
Малюнок 2. Тактильні рецептори у ссавців: шкірні тактильні рецептори диференціюються на нешкідливий дотик, який підтримується кількома рецепторами з низьким механічним порогом (LTMR) у голій і волосистій шкірі, і шкідливий дотик, який підтримується рецепторами з високим механічним порогом (HTMR). Вони утворюють вільні нервові закінчення, які закінчуються переважно в епідермісі. (A) Гола шкіра. A1: Тельця Мейснера виявляють рух шкіри та ковзання предмета в руці. Вони важливі для передачі предметів і спритності. Рецептори швидко адаптуються до подразника, з'єднані з А? волокон і розріджених до C волокон і мають велике рецепторне поле. A2: Тільця Руффіні виявляють розтягнення шкіри і є важливими для визначення положення пальців і предмета, що передається. Рецептор повільно адаптується до подразника і зберігає активність до тих пір, поки стимул застосовувався. Рецептори підключені до A? волокна і мають велике рецептивне поле. A3: Тільця Пачініа знаходяться глибше в дермі і виявляють вібрацію. Рецептори підключені до A? волокна; вони швидко адаптуються до подразника і мають найбільше рецептивне поле. (B) Ціла шкіра. B1: Комплекси клітин Меркель присутні як у голій шкірі, так і навколо волосся. Вони щільно виражені в руці і важливі для сприйняття текстури та найкращого розрізнення двох точок. Вони відповідають за точність пальців. Рецептори підключені до A? волокна; вони повільно адаптуються до подразника і мають коротке рецептивне поле. B2: Шкідливі дотику HTMR з дуже повільною адаптацією до стимулу, тобто активні, поки застосовується ноцицептивний стимул. Вони утворені вільним нервовим закінченням А? і С-волокна, пов'язані з кератиноцитами. (C) Волосата шкіра. C1: Волосяні фолікули пов'язані з різними типами волосся. У мишей Гвардієві волоски довші і рідко виражені, шило/ошень середнього розміру, а зигзагоподібні — найменші і найбільш густо виражені волоски. Вони пов’язані з А? волокон, але також до A? і C-LTMRs волокна для шила/ошена та зизагоподібного волосся. Вони розпізнають рух волосся, включаючи приємний дотик під час ласки. Вони швидко або з проміжною кінетичною адаптацією до подразника. C2: нервові закінчення C-touch відповідають підтипу закінчення C волокна з вільним закінченням, що характеризується низьким механічним порогом. Вони повинні кодувати приємні відчуття, викликані ласкою. Вони помірно пристосовуються до подразника і мають коротке рецептивне поле. Передбачувані механочутливі (MS) іонні канали, експресовані в різних тактильних рецепторах, вказані відповідно до попередніх даних і підсумовують наявну гіпотезу, що оцінюється.
Друга велика ідентифікована популяція стосується закінчень A?-LTMR у фолікулах Awl/Auchenne та зигзагоподібних фолікулів, які необхідно порівняти з волосяним фолікулом Down, детально вивченим у кішок і кроликів. Джінті та його співробітники показали, що TrkB експресується на високих рівнях у підгрупі нейронів DRG середнього діаметру. Внутрішньоклітинні записи з використанням мічених волокон шкірно-нервового препарату ex vivo показали, що вони виявляють фізіологічні властивості волокон, які раніше досліджували у кішок і кроликів: вишукану механічну чутливість (поріг фон Фрея < 0.07 мН), швидку адаптацію відповідей на надпорогові стимули, проміжну провідність. швидкості (5.8 × 0.9 м/с) і вузькі невигнуті шипи соми.15 Ці A?-LTMR утворюють поздовжні ланцетні закінчення, пов’язані практично з кожним зигзагоподібним та шиловидним/шиловидним волосяним фолікулом тулуба [рис. 1 (A5)].
Нарешті, вони показали, що периферичні закінчення швидко адаптуються A? LTMR утворюють поздовжні ланцетні закінчення, пов’язані з захисними (або тилотричними) і шило/аушеновими волосяними фолікулами [рис. 1 (A6)].15 Крім того, волоски Guard також пов'язані з комплексом клітин Меркель, що утворює сенсорний купол, з'єднаний з A? повільно адаптується LTMR [рис. 1 (A7)].
Таким чином, практично всі зигзагоподібні волосяні фолікули іннервуються як C-LTMR, так і A?-LTMR ланцетними закінченнями; волоски шила/ошені тричі іннервуються A? швидко адаптуються-LTMR, A?-LTMR і C-LTMR ланцетні закінчення; Охоронні волосяні фолікули іннервуються А? швидко адаптуються-LTMR поздовжні ланцетні закінчення і взаємодіють з A? повільна адаптація-LTMR закінчень сенсорного купола. Таким чином, кожен волосяний фолікул миші отримує унікальні та інваріантні комбінації закінчень LTMR, що відповідають нейрофізіологічно відмінним механосенсорним кінцевим органам. Беручи до уваги ітераційне розташування цих трьох типів волосся, Джінті та його співробітники припускають, що волохата шкіра складається з повторюваного повторення периферійної одиниці, що містить (1) один або два центрально розташованих захисних волоска, (2) ~20 оточуючих шило/ошень волосся і (3 ) ~80 вкраплених зигзагоподібних волосків [рис. 2 (C1)].
Проекція спинного мозку. Центральні проекції A? швидко адаптуються-LTMR, A?-LTMR і C-LTMR закінчуються в окремих, але частково перекриваються пластинках (II, III, IV) спинного рогу спинного мозку. Крім того, центральні термінали LTMR, які іннервують ті самі або сусідні волосяні фолікули в межах периферичної одиниці LTMR, вирівняні, щоб утворити вузький стовпець LTMR в спинному розі спинного мозку [рис. 1 (B1)]. Таким чином, ймовірно, що клин або стовпчик соматотопно організованих первинних сенсорних аферентних закінчень у дорсальному розі представляє вирівнювання центральних проекцій A?-, A?- і C-LTMR, які іннервують ту саму периферійну одиницю і виявляють механічні подразники, що діють на ту саму невелику групу волосяних фолікулів. Виходячи з кількості щитів, шила/ошень і зигзагоподібних волосків тулуба і кінцівок, а також кількості кожного підтипу LTMR, Джінті та його співробітники підрахували, що спинний ріг миші містить 2,000 4,000 × 15 XNUMX стовпців LTMR, що відповідає приблизній кількості стовпців LTMR. LTMR одиниці.XNUMX
Крім того, аксони підтипів LTMR тісно пов’язані один з одним, маючи переплетені виступи та переплетені ланцетні закінчення, які іннервують той самий волосяний фолікул. Крім того, оскільки три типи волосяних фолікулів мають різні форми, розміри та клітинний склад, вони, ймовірно, мають чіткі властивості відхилення або вібрації. Ці висновки узгоджуються з класичними нейрофізіологічними вимірюваннями у кішки та кролика, які вказують на те, що A? RA-LTMR і A?-LTMR можуть бути диференційовано активовані відхиленням різних типів волосяних фолікулів.16,17
На закінчення можна сказати, що дотик до волохатої шкіри є комбінацією: (1) відносної кількості, унікального просторового розподілу та чітких морфологічних і відхиляючих властивостей трьох типів волосяних фолікулів; (2) унікальні комбінації закінчень підтипу LTMR, пов'язаних з кожним із трьох типів волосяних фолікулів; і (3) чіткі чутливості, швидкості провідності, схеми стрибків і властивості адаптації чотирьох основних класів LTMR, пов'язаних з волосяними фолікулами, які дозволяють механосенсорній системі волосистої шкіри витягувати та передавати в ЦНС складні комбінації якостей, які визначають дотик.
Вільні нервові закінчення LTMR
Як правило, вільні закінчення C-волокон в шкірі є HTMR, але субпопуляція C-волокон не реагує на шкідливий дотик. Ця підгрупа тактильних аферентів C-волокна (CT) являє собою окремий тип немієлінових низькопорогових механорецепторних одиниць, які існують у волосистій, але не голій шкірі людей і ссавців [рис. 1 (A8)].18,19 КТ зазвичай асоціюються зі сприйняттям приємної тактильної стимуляції при тілесному контакті.20,21
Аференти КТ реагують на сили вдавлення в діапазоні 0.3÷2.5 мН і, таким чином, настільки ж чутливі до деформації шкіри, як і багато А? аференти.19 Адаптаційні характеристики аферентів СТ, таким чином, є проміжними в порівнянні з повільно та швидко адаптованими мієліновими механорецепторами. Рецептивні поля аферентів КТ людини мають приблизно круглу або овальну форму. Поле складається з від одного до дев’яти маленьких чутливих плям, розподілених на площі до 35 мм2.22. Рецептори гомологів миші організовані у вигляді неперервних плям, що охоплюють приблизно 50% площі волосистої шкіри [рис. 60 (C2)].2
Дані пацієнтів без мієлінових тактильних аферентів вказують на те, що передача сигналів у волокнах КТ активує острівну кору. Оскільки ця система погано кодує дискримінаційні аспекти дотику, але добре підходить для кодування повільного, ніжного дотику, волокна КТ в волосистій шкірі можуть бути частиною системи для обробки приємних і соціально значущих аспектів дотику.24 Активація КТ волокна також може бути частиною системи обробки приємних і соціально значимих аспектів дотику. грають роль у пригніченні болю, і нещодавно було припущено, що запалення або травма можуть змінити відчуття, що передаються LTMR C-волокна, від приємного дотику до болю.25,26
По якому шляху КТ-афференти рухаються, поки невідомо [рис. 1 (B2)], але були задокументовані низькопорогові тактильні введення в спиноталамічні проекційні клітини27, що підтверджує повідомлення про слабкі контралатеральні дефіцити виявлення дотику у пацієнтів після руйнування цих шляхів після процедури хордотомії.28
LTMR в гладкій шкірі
Клітинно-нейритні комплекси Меркель і сенсорний купол. Меркель (1875) був першим, хто дав гістологічний опис скупчень епідермальних клітин з великими часточковими ядрами, які контактують з передбачуваними аферентними нервовими волокнами. Він припустив, що вони підпорядковуються відчуттям дотику, називаючи їх Tastzellen (тактильні клітини). У людини клітинно-невритні комплекси Меркеля збагачені в чутливих до дотику ділянках шкіри, вони знаходяться в базальному шарі епідермісу на пальцях, губах і статевих органах. Вони також існують у волосистій шкірі з меншою щільністю. Клітинно-невритний комплекс Меркеля складається з клітини Меркеля, що знаходиться в тісному з’єднанні з збільшеним нервовим закінченням з одного мієлінізованого A? волокно [рис. 1 (C1)] (огляд у Halata та співробітників).29 На епідермальній стороні клітина Меркеля демонструє пальцеподібні відростки, що поширюються між сусідніми кератиноцитами [рис. 1 (C2)]. Клітини Меркеля — це епідермальні клітини, що походять із кератиноцитів.30,31 Термін «дотиковий купол» був введений, щоб назвати велику концентрацію клітинних комплексів Меркеля в волосистій шкірі передньої лапи кішки. Сенсорний купол може мати до 150 клітин Меркеля, іннервованих одним A?-волокном, а у людини, крім A?-волокон, A? і С-волокна також були регулярно присутні.32-34
Стимуляція клітинно-невритних комплексів Меркеля призводить до повільно адаптаційних реакцій типу I (SA I), які походять з пунктуальних рецептивних полів з різкими межами. Спонтанних виділень немає. Ці комплекси реагують на глибину вдавлення шкіри і мають найвищу просторову роздільну здатність (0.5 мм) шкірних механорецепторів. Вони передають точне просторове зображення тактильних стимулів і вважаються відповідальними за дискримінацію форми та текстури [рис. 2 (B1)]. Миші, позбавлені клітин Меркеля, не можуть виявити текстуровані поверхні своїми ногами, поки вони роблять це за допомогою вусів.35
Про те, чи клітина Меркель, сенсорний нейрон чи обидва є місцями механотрансдукції, досі залишається предметом дискусій. У щурів фототоксична деструкція клітин Меркеля скасовує відповідь SA I.36 У мишей із генетично пригніченими клітинами Меркель відповідь SA I, записаний in ex vivo підготовка шкіри/нерва, повністю зникає, демонструючи, що клітини Меркель необхідні для правильного кодування Меркель. рецепторні реакції.37 Однак механічна стимуляція ізольованих клітин Меркеля в культурі тиском, керованим двигуном, не генерує механічно керованих струмів.38,39 Кератиноцити можуть відігравати важливу роль у нормальному функціонуванні клітинно-невритного комплексу Меркеля. Пальцеподібні відростки клітини Меркеля можуть рухатися з деформацією шкіри та рухом клітин епідермісу, і це може бути першим кроком механічної трансдукції. Очевидно, що умови, необхідні для вивчення механочутливості клітин Меркеля, ще не встановлені.
Закінчення Руффіні. Закінчення Руффіні - це тонкі сигароподібні інкапсульовані сенсорні закінчення, з'єднані з A? нервові закінчення. Закінчення Руффіні являють собою невеликі циліндри сполучної тканини, розташовані вздовж дермальних колагенових ниток, які живляться від одного до трьох мієлінових нервових волокон діаметром 4 мкм. До трьох циліндрів різної орієнтації в дермі можуть зливатися, утворюючи один рецептор [рис. 6 (C1)]. За будовою закінчення Руффіні схожі на сухожильні органи Гольджі. Вони широко виражені в дермі і були ідентифіковані як шкірні механорецептори типу II (SA II), що повільно адаптуються. На тлі спонтанної нервової діяльності повільно адаптуються регулярні виділення викликаються перпендикулярним механічним подразненням з низькою силою або більш ефективно шляхом розтягування шкіри. Відповідь SA II походить від великих рецептивних полів з нечіткими кордонами. Рецептори Руффіні сприяють сприйняттю напрямку руху об'єкта через картину розтягування шкіри [рис. 3 (A2)].
У мишей реакції SA I та SA II можуть бути розділені електрофізіологічно під час препарування нервової шкіри ex-vivo.40 Нандасена та співробітники повідомили про імунолокалізацію аквапорину 1 (AQP1) у закінченнях періодонта Руффіні різців щурів, що припускає, що AQP1 бере участь у підтримання зубного осмотичного балансу, необхідного для механотрансдукції.41 Пародонтальні закінчення Руффіні також виражали ймовірний механочутливий іонний канал ASIC3.42
Тельця Мейснера. Тільця Мейснера локалізуються в дермальних сосочках голій шкіри, головним чином на долонях і підошвах ніг, а також на губах, на язиці, на обличчі, в сосках і на геніталіях. Анатомічно вони складаються з інкапсульованого нервового закінчення, капсула складається з сплощених підтримуючих клітин, розташованих у вигляді горизонтальних пластин, вбудованих у сполучну тканину. Є одне нервове волокно А? аференти, з'єднані в одне тільце [рис. 1 (C4)]. Будь-яка фізична деформація тільця викликає залп потенціалів дії, який швидко припиняється, тобто вони швидко адаптуються до рецепторів. Коли подразник видаляється, тільце відновлює свою форму і при цьому виробляє ще один залп потенціалів дії. Завдяки своєму поверхневому розташуванню в дермі ці тільця вибірково реагують на рух шкіри, тактильне виявлення ковзання та вібрації (20-40 Гц). Вони чутливі до динамічної шкіри – наприклад, між шкірою та об’єктом, з яким обробляють [рис. 2 (A1)].
Пачинові тільця. Пачинові тільця є глибокими механорецепторами шкіри і є найбільш чутливими інкапсульованими шкірними механорецепторами руху шкіри. Ці великі яйцевидні тільця (1 мм завдовжки), зроблені з концентричних пластин волокнистої сполучної тканини та фібробластів, вистелених плоскими модифікованими клітинами Шванна, експресуються в глибокій дермі.43 У центрі тільця, у заповненій рідиною порожнині, яка називається внутрішньою цибулиною. , закінчує один єдиний A? аферентне немієлінізоване нервове закінчення [рис. 1 (C5)]. Вони мають велике рецепторне поле на поверхні шкіри з особливо чутливим центром. Розвиток і функція кількох типів механорецепторів, які швидко адаптуються, порушені у мишей-мутантів c-Maf. Зокрема, тільця Пачіна сильно атрофовані.44
Тільця Пачініа виявляють дуже швидку адаптацію у відповідь на вдавлення шкіри, швидко адаптується II (RA II) нервовий розряд, який здатний слідувати високій частоті вібраційних подразників і дозволяє сприймати віддалені події через передані вібрації.45 Тільця Пачініа аференти реагують на тривале вдавлення перехідною активністю на початку і зміщенні стимулу. Їх також називають детекторами прискорення, оскільки вони можуть виявляти зміни в силі стимулу, і, якщо швидкість зміни стимулу змінюється (як це відбувається у вібраціях), їх реакція стає пропорційною цій зміні. Тільця Пачініа відчувають значні зміни тиску і найбільше вібрації (150-300 Гц), які вони можуть помітити навіть на відстані сантиметрів [рис. 2 (A3)].
Тонічну реакцію спостерігали в декапсульованому тільці Пачініа.46 Крім того, інтактні тільця Пачініа реагують постійною активністю під час постійних подразників, не змінюючи механічних порогів або частоти відповіді, коли опосередкована ГАМК сигналізація блокується між пластинчастою глією та нервовим закінченням.47 Таким чином, ненейронні компоненти тільця Пачіна можуть виконувати подвійну роль у фільтрації механічного стимулу, а також у модуляції властивостей реакції сенсорного нейрона.
Проекції спинного мозку. Проекції A?-LTMR в спинному мозку поділяються на дві гілки. Головна центральна гілка піднімається в спинному мозку в іпсилатеральних дорсальних стовпах до шийного рівня [рис. 1 (B3)]. Вторинні гілки закінчуються в дорсальному рогі в пластинках IV і перешкоджають передачі болю, наприклад. Це може послабити біль як частину контролю воріт [рис. 1 (B4)].48
На рівні шийки матки аксони головної гілки розділяються на два тракти: серединний тракт містить тонкий пучок, який передає інформацію від нижньої половини тіла (ноги і тулуб), а зовнішній тракт містить клиновидний пучок, який передає інформацію від верхньої половини. тіла (рук і тулуба) [рис. 1 (B5)].
Первинні тактильні аференти створюють свій перший синапс з нейронами другого порядку в мозковій речовині, де волокна з кожного тракту синапсу в однойменному ядрі: синапс аксонів gracile fasciculus в грацильному ядрі і синапс клиновидних аксонів у клиноподібному ядрі [рис. 1 (B6)]. Нейрони, які отримують синапс, забезпечують вторинні аференти і негайно перетинають середню лінію, щоб утворити тракт на контралатеральній стороні стовбура мозку – медіальний лемніс, який піднімається через стовбур мозку до наступної ретрансляційної станції в середньому мозку, зокрема, в таламус [рис. . 1 (B7)].
Молекулярна специфікація LTMR. Нещодавно були частково з’ясовані молекулярні механізми, що контролюють ранню диверсифікацію LTMR. Bourane та співробітники показали, що популяції нейронів, які експресують рецептор тирозинкінази Ret (Ret) та його корецептор GFR?2 у ембріональних мишей DRG E11�13, вибірково коекспресують транскрипційний фактор Mafa.49,50 Ці автори демонструють, що Mafa/ Нейрони Ret/GFR?2, призначені стати трьома специфічними типами LTRM при народженні: нейрони SA1, що іннервують комплекси клітин Меркель, нейрони, що швидко адаптуються, що іннервують тільця Мейснера, і швидко адаптуючі аференти (RA I), що утворюють ланцетні закінчення навколо волосяних фолікулів. Ginty та співробітники також повідомляють, що нейрони DRG, що експресують ранній Ret, швидко адаптують механорецептори з тілець Мейснера, тілець Пачіні та ланцетних закінчень навколо волосяних фолікулів.51 Вони іннервують дискретні цільові зони в межах грацильного та клиновидного ядер, виявляючи модифікаційний патерн mechanos. аксональні проекції нейронів у стовбурі мозку.
Дослідження механорецепторів шкіри людини. Техніка «мікроневрографії», описана Хагбартом і Валлбо в 1968 році, була застосована для вивчення поведінки розряду окремих механочутливих кінцівок людини, які живлять м’язи, суглоби і шкіру (див. огляд Macefield, 2005).52,53 Більшість мікронейрографії шкіри людини дослідження охарактеризували фізіологію тактильних аферентів у голій шкірі кисті. Записи мікроелектродів із серединного та ліктьового нервів у людей виявили відчуття дотику, що генеруються чотирма класами LTMR: аференти Мейснера особливо чутливі до легкого погладжування шкіри, реагуючи на локальні зусилля зсуву та початкові або явні ковзання в рецепторному полі. Аференти Пачініа надзвичайно чутливі до швидких механічних перехідних процесів. Аференти енергійно реагують на подування над рецептивним полем. Тільце Пачіна, розташоване в пальці, зазвичай реагує на постукування по столу, що підтримує руку. Аференти Меркеля, як правило, мають високу динамічну чутливість до стимулів вдавлення, нанесених на дискретну область, і часто реагують з відходом під час вивільнення. Хоча аференти Руффіні справді реагують на зусилля, які зазвичай прикладаються до шкіри, унікальною особливістю аферентів SA II є їх здатність реагувати також на бічні розтягування шкіри. Нарешті, волосяні одиниці на передпліччі мають великі яйцеподібні або неправильні рецептивні поля, що складаються з кількох чутливих плям, які відповідають окремим волоскам (кожне аферентне джерело ~20 волосків).
Механічна чутливість кератиноцитів
Будь-який механічний подразник на шкіру повинен передаватися через кератиноцити, які утворюють епідерміс. Ці повсюдно поширені клітини можуть виконувати сигнальні функції на додаток до своїх допоміжних або захисних функцій. Наприклад, кератиноцити виділяють АТФ, важливу сенсорну сигнальну молекулу, у відповідь на механічні та осмотичні подразники.54,55 Вивільнення АТФ викликає збільшення внутрішньоклітинного кальцію шляхом аутокринної стимуляції пуринергічних рецепторів.55 Крім того, є докази того, що гіпотонус активує Rho -кіназний сигнальний шлях і подальше утворення F-актинового стресового волокна, що свідчить про те, що механічна деформація кератиноцитів може механічно втручатися в сусідні клітини, такі як клітини Меркеля для нешкідливого дотику та вільні закінчення C-волокна для шкідливого дотику [рис. 1 (C6)].56,57
Шкідливий дотик
Високопороговими механорецепторами (HTMR) є епідермальні C- і A? вільні нервові закінчення. Вони не пов’язані зі спеціалізованими структурами і спостерігаються в обох волосистих шкірі [рис. 1 (A9)] і голі шкіри [рис. 1(C7)]. Однак термін вільних нервових закінчень слід розглядати з розумом, оскільки нервові закінчення завжди знаходяться в тісному зв’язку з кератиноцитами або клітинами Лангерана або меланоцитами. Ультраструктурний аналіз нервових закінчень виявляє наявність шорсткої ендоплазматичної сітки, рясні мітохондрії та щільно-ядерний пухир. Прилеглі мембрани епідермальних клітин потовщені і нагадують постсинаптичну мембрану в нервових тканинах. Зауважте, що взаємодія між нервовими закінченнями та клітинами епідермісу може бути двонаправленою, оскільки клітини епідермісу можуть вивільняти медіатори, такі як АТФ, інтерлейкін (IL6, IL10) та брадикінін, і навпаки, пептидергічні нервові закінчення можуть вивільняти пептиди, такі як CGRP або речовина P, що діють на клітини епідермісу. HTMR включають механоноцицептори, які збуджуються лише шкідливими механічними подразниками, і полімодальні ноцицептори, які також реагують на шкідливе тепло та екзогенні хімічні речовини [рис. 2 (В2)].58
Аферентні волокна HTMR закінчуються на проекційних нейронах у дорсальному розі спинного мозку. A?-HTMR контактують з нейронами другого порядку переважно в пластинках I і V, тоді як C-HTMR закінчуються в пластинці II [рис. 1 (B8)]. Ноцицептивні нейрони другого порядку проектуються на контрольну сторону спинного мозку і піднімаються в білу речовину, утворюючи передньолатеральну систему. Ці нейрони закінчуються переважно в таламусі [рис. 1 (B9 і B10)].
Механо-струми в соматосенсорних нейронах
Механізми повільної або швидкої адаптації механорецепторів ще не з’ясовані. Незрозуміло, якою мірою адаптація механорецепторів забезпечується клітинним середовищем чутливого нервового закінчення, внутрішніми властивостями механічно-керованих каналів і властивостями аксональних напругозалежних іонних каналів у сенсорних нейронах (рис. 2). Однак останній прогрес у характеристиці механічно-керованих струмів продемонстрував, що в нейронах DRG існують різні класи механочутливих каналів і можуть пояснити деякі аспекти адаптації механорецепторів.
Запис in vitro у гризунів показав, що сома нейронів DRG є внутрішньо механочутливою і експресує катіонні механокеровані струми.59-64 Гадоліній і рутенієвий червоний повністю блокують механочутливі струми, тоді як зовнішні кальцій і магній у фізіологічних концентраціях, а також амілорид і бензаміл, викликають часткову блокаду.60,62,63 FM1-43 діє як тривалий блокатор, а ін'єкція FM1-43 в задню лапу мишей знижує чутливість до болю в тесті Рендалла Селітто і підвищує оцінений поріг відведення лапи з волосками фон Фрея.65
У відповідь на тривалу механічну стимуляцію механочутливі струми зменшуються через замикання. На основі постійних часу спаду струму виділяють чотири різні типи механочутливих струмів: струми швидкої адаптації (~3 мс), проміжні адаптаційні струми (~6 мс), повільно адаптуючі струми (~15 мс). ) і надповільно адаптуються струми (~30 мс).200 Усі ці струми присутні з різною частотою в нейронах DRG щурів, що іннервують голу шкіру задньої лапи.300
Механічну чутливість механочутливих струмів можна визначити шляхом застосування ряду інкрементальних механічних подразників, що дає змогу проводити відносно детальний аналіз стимул-струм.66 Відношення стимул-струм зазвичай є сигмоїдальним, а максимальна амплітуда струму визначається кількістю канали, які одночасно відкриті.64,67 Цікаво, що швидко адаптуючий механочутливий струм, як повідомляється, демонструє низький механічний поріг і середню точку напівактивації порівняно з надповільно адаптованим механочутливим струмом.63,65
Сенсорні нейрони з неноцицептивними фенотипами переважно експресують механочутливі струми, що швидко адаптуються з нижчим механічним порогом. Це спонукало припустити, що ці струми можуть сприяти різним механічним порогам, які спостерігаються в LTMR і HTMR in vivo. Хоча до цих експериментів in vitro слід ставитися з обережністю, підтвердження присутності в сомі нейронів DRG низько- та високопорогових механотрансдюсерів також було надано завдяки радіальній стимуляції сенсорних нейронів миші на основі радіального розтягування.60,61,63,64,68 Ця парадигма виявила два основні популяції нейронів, чутливих до розтягування, один, який реагує на низьку амплітуду стимулу, а інший, який вибірково реагує на високу амплітуду стимулу.
Ці результати мають важливі, але спекулятивні, механістичні наслідки: механічний поріг сенсорних нейронів може не мати нічого спільного з клітинною організацією механорецептора, але може полягати у властивостях механічно закритих іонних каналів.
Нещодавно були розкриті механізми, що лежать в основі десенсибілізації механочутливих катіонних струмів у нейронах DRG щурів.64,67 Це є результатом двох одночасних механізмів, які впливають на властивості каналу: адаптації та інактивації. Вперше про адаптацію повідомлялося в дослідженнях слухових волоскових клітин. Операційно це можна описати як простий переклад кривої активації каналу датчика вздовж осі механічного стимулу.70-72 Адаптація дозволяє сенсорним рецепторам зберігати свою чутливість до нових подразників у присутності існуючого стимулу. Однак значна частина механочутливих струмів у нейронах DRG не може бути реактивована після кондиціонування механічної стимуляції, що вказує на інактивацію деяких каналів перетворювача.64,67 Отже, як інактивація, так і адаптація діють в тандемі для регулювання механочутливих струмів. Ці два механізми є загальними для всіх механочутливих струмів, ідентифікованих у нейронах DRG щурів, що свідчить про те, що пов’язані фізико-хімічні елементи визначають кінетику цих каналів.64
На закінчення можна сказати, що визначення властивостей ендогенних механочутливих струмів in vitro має вирішальне значення в пошуках механізмів трансдукції на молекулярному рівні. Змінність, що спостерігається в механічному порозі та кінетиці адаптації різних механічно-керованих струмів у нейронах DRG, припускає, що внутрішні властивості іонних каналів можуть пояснити, принаймні частково, механічний поріг та кінетику адаптації механорецепторів, описаних у десятиліттях 1960-х. 80 з використанням препаратів ex vivo.
Передбачувані механочутливі білки
Механочутливі іонні струми в соматосенсорних нейронах добре охарактеризовані, навпаки, мало відомо про ідентичність молекул, які опосередковують механотрансдукцію у ссавців. Генетичні скринінги у Drosophila і C. elegans виявили кандидати на механотрансдукцію молекул, включаючи сімейства TRP і дегенеринових/епітеліальних Na+-каналів (Deg/ENaC).73 Нещодавні спроби з’ясувати молекулярні основи механотрансдукції у ссавців були зосереджені переважно на цих гомологах-кандидатах. . Крім того, багато з цих кандидатів присутні в шкірних механорецепторах і соматосенсорних нейронах (рис. 2).
Кислотно-чутливі іонні канали
ASIC належать до протон-керованої підгрупи сімейства дегенерін-епітеліальних Na+-каналів.74 Три члени сімейства ASIC (ASIC1, ASIC2 і ASIC3) експресуються в механорецепторах і ноцицепторах. Роль каналів ASIC була досліджена в поведінкових дослідженнях на мишах з цілеспрямованою делецією генів каналів ASIC. Видалення ASIC1 не змінює функцію шкірних механорецепторів, але підвищує механічну чутливість аферентів, що іннервують кишечник.75 Нокаутні миші ASIC2 демонструють знижену чутливість швидко адаптованих шкірних LTMR.76 Однак наступні дослідження повідомили про відсутність ефектів від нокаутування ASIC2 на як вісцеральна механо-ноцицепція, так і шкірна механосенсація.77 Порушення ASIC3 зменшує механочутливість вісцеральних аферентів і зменшує реакцію шкірних HTMR на шкідливі подразники.76
Перехідний рецепторний канал
Надсімейство TRP підрозділяється на шість підсімейств у ссавців.78 Майже всі підродини TRP мають членів, пов’язаних з механочутливістю в різноманітних клітинних системах.79 Однак у сенсорних нейронах ссавців канали TRP найбільш відомі для виявлення теплової інформації та медіації нейрогенного запалення, і лише два канали TRP, TRPV4 і TRPA1, були задіяні в чутливості до дотику. Порушення експресії TRPV4 у мишей має лише незначний вплив на гострі механосенсорні пороги, але сильно знижує чутливість до шкідливих механічних подразників.80,81 TRPV4 є вирішальною детермінантою у формуванні реакції ноцицептивних нейронів на осмотичний стрес і механічну гіпералгезію.82,83 під час запалення1, ммм. 1 Здається, TRPA1 відіграє роль у механічній гіпералгезії. Миші з дефіцитом TRPA84,85 виявляють гіперчутливість до болю. TRPAXNUMX сприяє передачі механічних, холодових і хімічних подразників у сенсорних нейронах ноцицепторів, але, здається, це не є важливим для трансдукції волоскових клітин.XNUMX
Немає чітких доказів того, що канали TRP і канали ASIC, виражені у ссавців, механічно закриті. Жоден з цих каналів, виражених гетерологічно, не повторює електричну сигнатуру механочутливих струмів, що спостерігаються в їхньому рідному середовищі. Це не виключає можливості того, що канали ASIC і TRP є механопреобразователями, враховуючи невизначеність того, чи може канал механотрансдукції функціонувати за межами свого клітинного контексту (див. розділ SLP3).
П'єзопротеїни
Косте і його співробітники нещодавно визначили п'єзобілки як перспективних кандидатів на механосенсорні білки.86,87 У хребетних є два члени п'єзо, Piezo 1 і Piezo 2, раніше відомі як FAM38A і FAM38B, відповідно, які добре збережені в багатоклітинному еуку. . П’єзо 2 міститься у великій кількості в ДРГ, тоді як П’єзо 1 ледве виявляється. П'єзоіндуковані механочутливі струми запобігаються пригніченню гадолінієм, рутенієвим червоним і GsMTx4 (токсин тарантула Grammostola spatulata).88 Експресія Piezo 1 або Piezo 2 в гетерологічних системах викликає механочутливі струми, кінетика струму Piezoer2 є швидкою. ніж П’єзо 1. Подібно до ендогенних механочутливих струмів, п’єзозалежні струми мають реверсивні потенціали близько 0 мВ і не є катіонними неселективними, при цьому Na+, K+, Ca2+ і Mg2+ всі пронизують основний канал. Аналогічно, п'єзозалежні струми регулюються мембранним потенціалом з помітним уповільненням кінетики струму при деполяризованих потенціалах.86
П'єзо-білки, безсумнівно, є механочутливими білками і мають багато властивостей швидко адаптованих механочутливих струмів у сенсорних нейронах. Обробка культивованих нейронів DRG короткою інтерферуючою РНК Piezo 2 зменшила частку нейронів із струмом, що швидко адаптується, та зменшила відсоток механочутливих нейронів.86 Трансмембранні домени розташовані по всьому п’єзобілкам, але очевидних мотивів, що містять пори, чи сигнатур іонних каналів не було. ідентифікований. Однак мишачий білок Piezo 1, очищений та відновлений в асиметричні ліпідні двошари та ліпосоми, утворює іонні канали, чутливі до рутенієвого червоного.87 Важливим кроком у перевірці механотрансдукції через п’єзо-канали є використання підходів in vivo для визначення функціональної важливості передачі сигналів дотику. Інформація була надана в Drosophila, де видалення одного члена Piezo зменшувало механічну реакцію на шкідливі подразники, не впливаючи на нормальний дотик.89 Хоча їх структура ще належить визначити, це нове сімейство механочутливих білків є багатообіцяючим предметом для майбутніх досліджень за межами кордону. відчуття дотику. Наприклад, нещодавнє дослідження пацієнтів з анемією (спадковий ксероцитоз) показує роль Piezo 1 у підтримці гомеостазу об’єму еритроцитів.90
Трансмембранний канал-подібний (TMC)
Нещодавнє дослідження вказує на те, що два білки, TMC1 і TMC2, необхідні для механотрансдукції волоскових клітин.91 Повідомлялося про спадкову глухоту через мутацію гена TMC1 у людей і мишей.92,93 Наявність цих каналів ще не виявлено в соматосенсорній системі. , але це, здається, хороший підказок для розслідування.
Стоматиноподібний білок 3 (SLP3)
На додаток до каналів трансдукції, було показано, що деякі допоміжні білки, пов’язані з каналом, відіграють роль у чутливості до дотику. SLP3 експресується в нейронах DRG ссавців. Дослідження з використанням мутантних мишей без SLP3 показали зміну механочутливості та механочутливих струмів.94,95 Точна функція SLP3 залишається невідомою. Він може бути лінкером між механочутливим каналом і основними мікротрубочками, як запропоновано для його гомолога C. elegans MEC2.96 Нещодавно GR. Лабораторія Левіна припустила, що прив’язка синтезується сенсорними нейронами DRG і пов’язує механочутливий іонний канал із позаклітинним матриксом.97 Порушення зв’язку скасовує RA-механочутливий струм, що свідчить про те, що деякі канали іонів є механочутливими лише тоді, коли вони прив’язані. RA-механочутливі струми також інгібуються ламінін-332, матричним білком, що продукується кератиноцитами, що підтверджує гіпотезу про модуляцію механочутливого струму позаклітинними білками.98
Підсімейство каналів K+
Паралельно з катіонними деполяризуючими механочутливими струмами досліджується наявність реполяризаційних механочутливих K+ струмів. K+-канали в механочутливих клітинах можуть переходити в поточний баланс і сприяти визначенню механічного порогу та часу адаптації механорецепторів.
Члени KCNK належать до сімейства каналів K+ з двома порами (K2P).99,100 K2P демонструє чудовий діапазон регуляції клітинними, фізичними та фармакологічними агентами, включаючи зміни pH, нагрівання, розтягування та деформацію мембрани. Ці K2P активні при мембранному потенціалі спокою. Кілька субодиниць KCNK експресуються в соматосенсорних нейронах.101 Канали KCNK2 (TREK-1), KCNK4 (TRAAK) і TREK-2 є одними з небагатьох каналів, для яких було показано пряме механічне гальмування шляхом розтягування мембрани.102,103
Миші з порушеним геном KCNK2 демонстрували підвищену чутливість до тепла та слабких механічних подразників, але нормальний поріг відміни шкідливого механічного тиску, прикладеного до задньої лапи за допомогою тесту Рендалла Селітто. умови. Нокаутні миші KCNK104 були гіперчутливі до легкої механічної стимуляції, і ця гіперчутливість була збільшена додатковою інактивацією KCNK2 Підвищена механочутливість цих нокаутних мишей може означати, що розтягнення зазвичай активує як деполяризуючі, так і реполяризуючі механочутливі струми, подібно до некоординованого механочутливого струму. деполяризуючі та реполяризуючі вольт-залежні струми.
KCNK18 (TRESK) є основним фактором фонової K+ провідності, яка регулює потенціал мембрани спокою соматосенсорних нейронів.106 Хоча невідомо, чи KCNK18 безпосередньо чутливий до механічної стимуляції, він може відігравати роль у опосередковуванні відповідей на легкий дотик, а також хворобливі механічні подразники. Вважається, що KCNK18 і в меншій мірі KCNK3 є молекулярною мішенню гідрокси-?-sanshool, сполуки, знайденої в горошку перцю Шезуан, яка активує рецептори дотику та викликає відчуття поколювання у людей.107,108
Залежний від напруги K+-канал KCNQ4 (Kv7.4) має вирішальне значення для встановлення переваги швидкості та частоти субпопуляції механорецепторів, які швидко адаптуються як у мишей, так і у людей. Мутація KCNQ4 спочатку була пов’язана з формою спадкової глухоти. Цікаво, що нещодавнє дослідження локалізує KCNQ4 в периферичних нервових закінченнях шкірного волосяного фолікула і тільця Мейснера. Відповідно, втрата функції KCNQ4 призводить до вибіркового посилення чутливості механорецепторів до низькочастотної вібрації. Примітно, що люди з пізньою втратою слуху через домінантну мутацію гена KCNQ4 демонструють підвищену продуктивність у виявленні низькочастотної вібрації малої амплітуди.109

Інсайт доктора Алекса Хіменеса
Дотик вважається одним із найскладніших почуттів в людському тілі, особливо тому, що за це не відповідає ніякий певний орган. Замість цього відчуття дотику відбувається через сенсорні рецептори, відомі як механорецептори, які знаходяться по всій шкірі і реагують на механічний тиск або спотворення. У голій, або безволосій шкірі ссавців є чотири основних типи механорецепторів: пластинчасті тільця, тактильні тільця, нервові закінчення Меркеля і цибулинні тільця. Механорецептори функціонують для виявлення дотику, для контролю положення м’язів, кісток і суглобів, відомих як пропріоцепція, і навіть для виявлення звуків і руху тіла. Розуміння механізмів структури та функції цих механорецепторів є основним елементом у використанні методів лікування та лікування болю.
Висновок
Дотик є складним відчуттям, оскільки він представляє різні тактильні якості, а саме вібрацію, форму, текстуру, задоволення та біль, з різними дискримінаційними характеристиками. До цього часу відповідність між органом дотику і психофізичним відчуттям була корелятивною, і специфічні для класу молекулярні маркери тільки з'являються. Зараз необхідна розробка тестів на гризунах, які б відповідали різноманітності поведінки на дотик, щоб полегшити майбутню ідентифікацію геноміки. Використання мишей, у яких відсутні певні підгрупи сенсорних аферентних типів, значно полегшить ідентифікацію механорецепторів і сенсорних аферентних волокон, пов’язаних з певною модальністю дотику. Цікаво, що нещодавня стаття відкриває важливе питання про генетичну основу механосенсорних ознак у людини і припускає, що мутація одного гена може негативно вплинути на чутливість до дотику.110 Це підкреслює, що патофізіологія дефіциту дотику людини значною мірою невідома і, безсумнівно, прогресувати шляхом точного визначення підгрупи сенсорних нейронів, пов’язаних з модальністю дотику або дефіцитом дотику.
У свою чергу, було досягнуто прогресу у визначенні біофізичних властивостей механізованих струмів.64 Розвиток останніх років нових методів, що дозволяють відстежувати зміни натягу мембрани під час запису механізованого струму, виявився цінним експериментальним методом для опису механочутливі струми зі швидкою, проміжною та повільною адаптацією (огляд Delmas та співробітників).66,111 Майбутнім буде визначення ролі властивостей струму в механізмах адаптації функціонально різноманітних механорецепторів і внеску механочутливих K+-струмів у збудливість LTMR і HTMR.
Молекулярна природа механо-керованих струмів у ссавців також є перспективною темою дослідження. Майбутні дослідження будуть просуватися в двох аспектах, спочатку для визначення ролі додаткової молекули, яка зв’язує канали з цитоскелетом і буде потрібною для надання або регулювання механочутливості іонних каналів подібних сімейств TRP і ASIC/EnaC. По-друге, дослідити велику та багатообіцяючу сферу внеску п’єзо-каналів, відповівши на ключові питання, що стосуються механізмів проникнення та ґратування, підмножини сенсорних нейронів та дотику, що залучають П’єзо, та ролі П’єзо в ненейронних клітинах, пов’язаних із механочутливість.
Відчуття дотику, порівняно з зір, смак, звук і нюх, які використовують специфічні органи для обробки цих відчуттів, можуть виникати по всьому тілу через крихітні рецептори, відомі як механорецептори. Різні типи механорецепторів можна знайти в різних шарах шкіри, де вони можуть виявляти широкий спектр механічних подразників. У статті вище описані конкретні моменти, які демонструють розвиток структурно-функціональних механізмів механорецепторів, пов’язаних з дотиком. Інформація з посиланням на Національний центр біотехнологічної інформації (NCBI). Обсяг нашої інформації обмежений хіропрактикою, а також травмами та станами хребта. Щоб обговорити тему, зверніться до доктора Хіменеса або зв’яжіться з нами за адресою�915-850-0900.
Куратор доктор Алекс Хіменес
Додаткові теми: Біль у спині
Біль у спині є однією з найпоширеніших причин інвалідності та пропущених робочих днів у всьому світі. Насправді, біль у спині вважається другою за поширеністю причиною відвідувань лікаря, переважаючи лише інфекції верхніх дихальних шляхів. Приблизно 80 відсотків населення відчувають біль у спині принаймні один раз протягом життя. Хребет – це складна структура, що складається з кісток, суглобів, зв’язок і м’язів, а також інших м’яких тканин. Через це травми та/або загострення стану, наприклад грижі диски, може зрештою призвести до симптомів болю в спині. Спортивні травми або травми в автомобільній катастрофі часто є найчастішою причиною болю в спині, однак іноді найпростіші рухи можуть мати хворобливі наслідки. На щастя, альтернативні варіанти лікування, такі як хіропрактика, можуть допомогти полегшити біль у спині за допомогою корекції хребта та ручних маніпуляцій, що в кінцевому підсумку покращує полегшення болю.

ДОДАТКО ВАЖЛИВА ТЕМА: Лікування болю в попереку
ІНШЕ ТЕМ: ДОДАТКОВО: Хронічний біль і лікування
Бланк
посилання
Закрити акордеон
Інформація в цьому документі на "Структурно-функціональні механізми механорецепторів" не призначений для заміни особистих стосунків із кваліфікованим медичним працівником або ліцензованим лікарем і не є медичною консультацією. Ми заохочуємо вас приймати рішення щодо охорони здоров’я на основі ваших досліджень і партнерства з кваліфікованим медичним працівником.
Інформація в блозі та обговорення обсягу
Наша інформаційна сфера обмежується хіропрактикою, опорно-руховим апаратом, фізичними препаратами, оздоровленням, що сприяє етіологічному вісцеросоматичні порушення у клінічних презентаціях, клінічній динаміці асоційованого соматовісцерального рефлексу, комплексах підвивиху, чутливих питаннях здоров’я та/або статей, темах та дискусіях з функціональної медицини.
Надаємо та презентуємо клінічне співробітництво з фахівцями різних галузей. Кожен фахівець керується своєю професійною сферою практики та юрисдикцією ліцензування. Ми використовуємо протоколи функціонального здоров’я та оздоровлення для лікування та підтримки догляду за травмами або розладами опорно-рухового апарату.
Наші відео, дописи, теми, предмети та висновки охоплюють клінічні питання, проблеми та теми, які стосуються та прямо чи опосередковано підтримують нашу клінічну практику.*
Наш офіс обґрунтовано намагався надати підтверджувальні цитати та визначив відповідне дослідження або дослідження, що підтверджують наші публікації. За запитом ми надаємо копії допоміжних наукових досліджень, доступні регуляторним комісіям та громадськості.
Ми розуміємо, що ми розглядаємо питання, які потребують додаткового пояснення того, як це може допомогти в певному плані догляду або протоколі лікування; тому для подальшого обговорення вищезазначеної теми, будь ласка, не соромтеся запитувати Доктор Алекс Хіменес, округ Колумбія, Або зв'яжіться з нами за адресою 915-850-0900.
Ми тут, щоб допомогти вам та вашій родині.
Благословення
Д-р Алекс Хіменес Постійного струму, MSACP, RN*, CCST, IFMCP*, CIFM*, ATN*
електронна пошта: coach@elpasofunctionalmedicine.com
Ліцензія доктора хіропрактики (DC) у Техас & Нью-Мексико*
Техас, округ Колумбія, номер ліцензії TX5807, Нью-Мексико, округ Колумбія Номер ліцензії NM-DC2182
Ліцензія дипломованої медсестри (RN*) in Флорида
Ліцензія Флориди Ліцензія RN # RN9617241 (Контрольний номер 3558029)
Компактний статус: Мультидержавна ліцензія: Уповноважений на практику в Стани 40*
Доктор Алекс Хіменес, округ Колумбія, MSACP, RN* CIFM*, IFMCP*, ATN*, CCST
Моя цифрова візитна картка







